Keton cisimlərinin çoxölçülü rolu
Keton cisimləri qaraciyər tərəfindən yaradılır və qlükoza insan orqanizmində asanlıqla mövcud olmadığı zaman enerji mənbəyi kimi istifadə olunur. İki əsas keton cismi asetoasetat (AcAc) və 3-beta-hidroksibutiratdır (3HB), aseton isə üçüncü və ən az bol olan keton cismidir. Ketonlar həmişə qanda olur və onların səviyyəsi oruc və uzunmüddətli məşq zamanı artırKetogenesis orqanizmlərin keton orqanlarını yağ turşuları və ketogenik amin turşuları ilə çıxardığı biyokimyəvi prosesdir.
Keton cəsədləri əsasən yaradılıb qaraciyər hüceyrələrinin mitokondriyası. Ketogenez qanda az glikoz səviyyələri olduqda baş verir, xüsusilə glikogen kimi digər hüceyrə karbonhidratlı maddələrdən sonra tükənmiş olur. Bu mexanizm kifayət qədər insulin miqdarında olmadıqda da baş verə bilər. Keton cismlərinin istehsalı, nəticədə, insan orqanında yağ turşuları olaraq saxlanılan enerjinin mövcud olması üçün başlamışdır. Ketogenez, müstəqil tənzimləndiyi mitokondriyalarda baş verir.
mücərrəd
Keton cisim metabolizmi fizioloji homeostazın mərkəzi bir nüvəsidir. Bu nəzərdən keçirildikdə, ketonların müxtəlif növ qida maddələrində orqan və orqanizmin performansını optimallaşdırmaq və çoxlu orqan sistemlərində iltihablanma və yaralanmalardan qorunması üçün ayrılmış ince tuning metabolik rolları necə işlədiyini müzakirə edirik. Ənənəvi olaraq karbohidrat məhdudlaşdırılmasında metabolik substratlar kimi baxılır, son müşahidələr karbonhidratlar bol olduğunda keton orqanlarının vacib metabolik və sinyal mediatorları kimi əhəmiyyətini vurğulayır. Sinir sisteminin xəstəlikləri üçün bilinən müalicə variantlarının repertuarını tamamlayan, kasıb orqanlarının kanser orqanlarının potensial rolları, ürək və qaraciyərdə maraqlı qoruma rolları, obezite ilə bağlı və ürək-damar xəstəliyində müalicə variantlarının açılması kimi yaranmışdır. Keton metabolizması və siqnalizasiya mövzusundakı mübahisələr, müasir müşahidələrlə klassik dogma ilə barışmaq üçün müzakirə edilir.
giriş
Keton cisimləri həyatın bütün sahələri, eukarya, bakteriya və arxeya üçün həyati vacib alternativ metabolik yanacaq mənbəyidir (Aneja et al., 2002; Cahill GF Jr, 2006; Krishnakumar et al., 2008). İnsanlarda keton bədən metabolizması, qida çatışmazlığının epizodik dövrlərində beyni yanacaq üçün istifadə edilmişdir. Keton cisimləri ?-oksidləşmə (FAO), trikarboksilik turşu dövrü (TCA), qlükoneogenez, de novo lipogenez (DNL) və sterolların biosintezi kimi mühüm məməlilərin metabolik yolları ilə birləşir. Məməlilərdə keton cisimləri əsasən qaraciyərdə FAO-dan əldə edilən asetil-KoA-dan istehsal olunur və onlar terminal oksidləşmə üçün qaraciyərdənkənar toxumalara daşınır. Bu fiziologiya, yağ turşularının mövcudluğunu artıran və karbohidratların mövcudluğunu azaldan nisbətən qısa oruc müddətləri ilə artırılan alternativ yanacaq təmin edir (Cahill GF Jr, 2006; McGarry və Foster, 1980; Robinson və Williamson, 1980). Keton bədəninin oksidləşməsi, oruc, aclıq, neonatal dövr, məşqdən sonrakı, hamiləlik və aşağı karbohidratlı pəhrizlərə riayət daxil olmaqla, çoxsaylı fizioloji vəziyyətlərdə ekstrahepatik toxumalarda məməlilərin ümumi enerji mübadiləsinə əhəmiyyətli töhfə verir. Sağlam yetkin insanlarda dövran edən ümumi keton cisim konsentrasiyası normal olaraq təxminən 100-250 µM arasında sirkadiyalı salınımlar nümayiş etdirir, uzunmüddətli məşqdən və ya 1 saatlıq aclıqdan sonra ~24 mM-ə qədər yüksəlir və diabetik ketoasidoz kimi patoloji vəziyyətlərdə 20 mM-ə qədər toplana bilər. Cahill GF Jr, 2006; Johnson et al., 1969b; Koeslag et al., 1980; Robinson and Williamson, 1980; Wildenhoff et al., 1974). İnsan qaraciyəri gündə 300 q-a qədər keton cisimcikləri istehsal edir (Balasse və Fery, 1989), bu da qidalanma, aclıq və aclıq vəziyyətlərində ümumi enerji xərclərinin 5-20%-ni təşkil edir (Balasse et al., 1978; Cox et al. al., 2016).
Son tədqiqatlar indi memeli hüceyrələrinin maddələr mübadiləsində, homeostazda və müxtəlif fizioloji və patoloji hallarda sinonoid orqanlarında vacib rol oynayır. Beyin, ürək və ya skelet əzələsi kimi ekstrahepatik toxumalar üçün enerjili yanacaqlar kimi xidmət göstərənlərdən başqa, keton orqanları sinyal mediatorları, protein post-translational modifikasiyası (PTM) sürücüsü və iltihab və oksidləşdirici stressin modulatorları kimi mühüm rol oynayır. Bu nəzəriyyədə biz Keto orqanlarının və onların metabolizmasının pleiotrop rollarının klassik və müasir baxışlarını təmin edirik.
Keton Bədən Metabolizmasına Baxış
Qaraciyər ketogenezinin sürəti yağın fizioloji və biokimyəvi transformasiyalarının təşkil edilmiş seriyası ilə idarə olunur. İlkin tənzimləyicilərə triaçilqliserollardan yağ turşularının lipolizi, hepatosit plazma membranına daşınması, karnitin palmitoiltransferaza 1 (CPT1) vasitəsilə mitoxondriyaya daşınması, β-oksidləşmə spiralı, TCA dövrünün aktivliyi və aralıq konsentrasiyalar, redoks potensialı və requlator daxildir. bu proseslərdən, əsasən qlükaqon və insulin [nəzərdən keçirilmişdir (Arias və digərləri, 1995; Ayte və digərləri, 1993; Ehara və digərləri, 2015; Ferre və digərləri, 1983; Kahn və digərləri, 2005; McGarry və Foster). , 1980; Williamson et al., 1969)]. Klassik olaraq ketogenez, ?-oksidləşmədən əldə edilən asetil-KoA-nın sitrat sintaza aktivliyini və/və ya sitrat əmələ gətirmək üçün kondensasiya üçün oksaloasetatın mövcudluğunu üstələyən yayılma yolu kimi nəzərdən keçirilir. Üç karbonlu ara məhsullar, ehtimal ki, asetil-KoA istehlakı üçün oksaloasetat hovuzunu genişləndirmək qabiliyyətinə görə anti-ketogenik fəaliyyət göstərir, lakin qaraciyərdə asetil-KoA konsentrasiyası tək başına ketogenik dərəcəsini təyin etmir (Foster, 1967; Rawat və Menahan, 1975; Williamson və başqaları, 1969). Ketogenezin hormonal, transkripsiya və post-tərcümə hadisələri ilə tənzimlənməsi birlikdə ketogenik sürəti tənzimləyən molekulyar mexanizmlərin tam başa düşülmədiyi fikrini dəstəkləyir (bax HMGCS2 və SCOT/OXCT1 Tənzimlənməsi).
Ketogenez ilk növbədə qaraciyərin mitoxondrial matrisində ümumi yağ oksidləşməsinə mütənasib sürətlə baş verir. Asil zəncirlərinin mitoxondrial membranlar vasitəsilə daşınmasından və ?-oksidləşmədən sonra, 3-hidroksimetilqlutaril-KoA sintazasının (HMGCS2) mitoxondrial izoformu asetoasetil-CoA (AcAc-CoA) kondensasiyasına səbəb olan taleyi kataliz edir və H-M-CoA-nı əmələ gətirir. (Şəkil 1A). HMG-CoA liazası (HMGCL) asetil-KoA və asetoasetatı (AcAc) azad etmək üçün HMG-CoA-nı parçalayır və sonuncu fosfatidilkolindən asılı mitoxondrial dehidrogenaz (D-OHB) tərəfindən d-?-hidroksibutirata (d-?OHB) çevrilir. BDH1) NAD+/NADH ilə birləşmiş tarazlığa yaxın reaksiyada (Bock və Fleischer, 1975; LEHNINGER et al., 1960). BDH1 tarazlıq sabiti d-?OHB istehsalına üstünlük verir, lakin AcAc/d-?OHB keton cisimlərinin nisbəti mitoxondrial NAD+/NADH nisbəti ilə düz mütənasibdir və beləliklə, BDH1 oksidoreduktaz fəaliyyəti mitoxondrial redoks potensialını modullaşdırır (Krebs və digərləri, 1969; Williamson və başqaları, 1967). AcAc həmçinin ketoasidozdan əziyyət çəkən insanlarda şirin qoxu mənbəyi olan asetona (Pedersen, 1929) kortəbii olaraq dekarboksilə çevrilə bilər (yəni, ümumi serum keton cisimləri > ~7 mM; AcAc pKa 3.6, ?OHB pKa 4.7). Keton cisimlərinin mitoxondrial daxili membran vasitəsilə daşınması mexanizmləri məlum deyil, lakin AcAc/d-?OHB hüceyrələrdən monokarboksilat daşıyıcıları (məməlilərdə, MCT 1 və 2, həmçinin məhlul daşıyıcısı 16A ailə üzvləri 1 və 7) və dövriyyədə terminal oksidləşmə üçün ekstrahepatik toxumalara daşınır (Cotter və digərləri, 2011; Halestrap və Wilson, 2012; Halestrap, 2012; Hugo et al., 2012). Sirkulyasiya edən keton cisimlərinin konsentrasiyası ekstrahepatik toxumalarda olandan daha yüksəkdir (Harrison və Long, 1940) bu, keton cisimlərinin konsentrasiya qradiyenti ilə aşağı daşındığını göstərir. MCT1-də funksiya itkisi mutasiyaları kortəbii ketoasidoz hücumları ilə əlaqələndirilir və keton cisimlərinin idxalında mühüm rol oynayır.
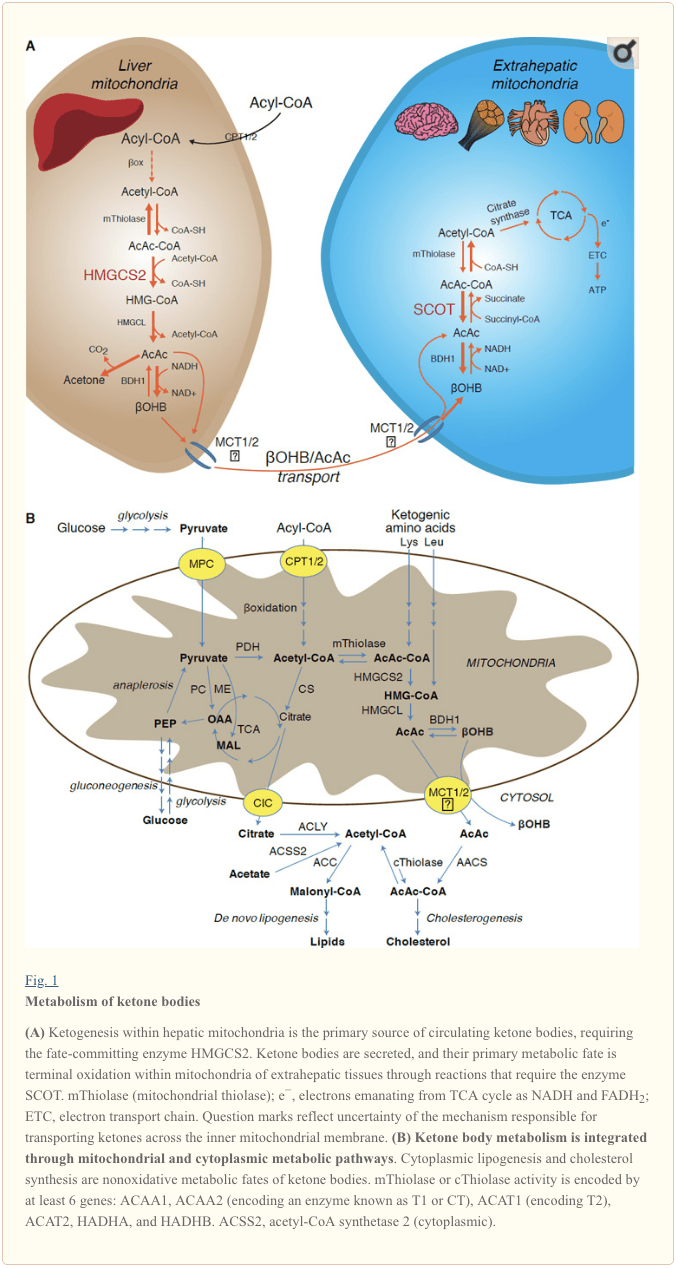
Keton cisimlərinin qeyri-oksidləşdirici talelərə çevrilməsi istisna olmaqla (bax: Keton cisimlərinin oksidləşdirici olmayan metabolik taleyi), hepatositlər istehsal etdikləri keton cisimlərini metabolizə etmək qabiliyyətinə malik deyillər. Qaraciyər tərəfindən de novo sintez edilən keton cisimləri (i) qaraciyərdənkənar toxumaların mitoxondrilərində terminal oksidləşmə üçün TCA dövrü üçün mövcud olan asetil-KoA-ya katabolize olur (Şəkil 1A), (ii) lipogenez və ya sterol sintezi yollarına yönləndirilir ( Şəkil 1B) və ya (iii) sidikdə ifraz olunur. Alternativ enerji yanacağı kimi keton cisimləri ürək, skelet əzələsi və beyində ehtirasla oksidləşir (Balasse və Fery, 1989; Bentourkia və s., 2009; Owen və digərləri, 1967; Reichard və digərləri, 1974; Sultan, 1988). ). Ekstrahepatik mitoxondrial BDH1, OHB oksidləşməsinin ilk reaksiyasını kataliz edir, onu geri AcAc-ə çevirir (LEHNINGER və digərləri, 1960; Sandermann və digərləri, 1986). BDH2-ə yalnız 20% ardıcıl eyniliyi olan sitoplazmik d-?OHB-dehidrogenaz (BDH1) keton cisimləri üçün yüksək Km-ə malikdir və həmçinin dəmir homeostazında rol oynayır (Davuluri və digərləri, 2016; Guo və digərləri, 2006) . Qaraciyərdənkənar mitoxondrial matrisdə AcAc unikal məməli KoA transferazı, suksinil-CoA:3-oksoacid-CoA transferaz (SCOT, CoA transferaz) tərəfindən kataliz edilən reaksiyada suksinil-KoA-dan CoA-yarımının mübadiləsi yolu ilə AcAc-CoA-ya aktivləşdirilir; OXCT1 ilə kodlanmış), yaxın tarazlıq reaksiyası vasitəsilə. AcAc-CoA-nın hidrolizi ilə ayrılan sərbəst enerji süksinil-CoA-dan daha böyükdür və AcAc əmələ gəlməsinə üstünlük verir. Beləliklə, keton cisimlərinin oksidləşdirici axını kütləvi təsirə görə baş verir: bol AcAc tədarükü və sitrat sintaza vasitəsilə asetil-KoA-nın sürətli istehlakı SCOT tərəfindən AcAc-CoA (+ süksinat) əmələ gəlməsinə kömək edir. Qeyd etmək lazımdır ki, qlükoza (heksokinaza) və yağ turşularından (asil-CoA sintetazalarından) fərqli olaraq, keton cisimlərinin (SCOT) oksidləşə bilən formada aktivləşməsi ATP investisiyasını tələb etmir. Geri dönən AcAc-CoA tiolaza reaksiyası [ACAA2 (T1 və ya CT kimi tanınan fermenti kodlayan), ACAT1 (T2 kodlayan), HADHA və ya HADHB ilə kodlanan dörd mitoxondrial tiolazadan hər hansı biri tərəfindən kataliz edilir] iki molekul asetil-CoA verir. TCA dövrünə daxil olan (Hersh və Jencks, 1967; Stern et al., 1956; Williamson et al., 1971). Ketotik vəziyyətlər zamanı (yəni, ümumi serum ketonları > 500 µM) keton cisimləri enerji xərclərinin əhəmiyyətli töhfələrinə çevrilir və oksidləşmənin udulması və ya doyması baş verənə qədər toxumalarda sürətlə istifadə olunur (Balasse və digərləri, 1978; Balasse və Fery, 1989). Edmond və başqaları, 1987). Qaraciyərdən əldə edilən keton cisimlərinin çox kiçik bir hissəsi sidikdə asanlıqla ölçülə bilər və böyrəklər tərəfindən istifadə və reabsorbsiya dərəcələri dövran edən konsentrasiyaya mütənasibdir (Goldstein, 1987; Robinson və Williamson, 1980). Yüksək ketotik vəziyyətlərdə (plazmada > 1 mM) ketonuriya ketozun yarı kəmiyyətli məruzəçisi kimi xidmət edir, baxmayaraq ki, sidikdə keton cisimlərinin əksər klinik analizləri AcAc-i aşkar edir, lakin ?OHB-ni aşkar etmir (Klocker et al., 2013).
Ketogenik substratlar və Hepatosit metabolizmasına təsirləri
Ketogenik substratlar yağ turşuları və amin turşuları (Şəkil 1B) daxildir. Amin turşularının, xüsusən lösinlərin katabolizmi post-absorbsiyalı vəziyyətdə keton orqanlarının xNUMX% -ni təşkil edir (Thomas və digərləri, 4). Belə ki, keton orqanlarını yaratmaq üçün asetil-COA substrat hövzəsi əsasən yağ turşularından yaranır, çünki azalmış karbohidrat tədarükü şəraitində piruvat əsasən anapleroz, yəni oksaloasetata (OAA) ATP-qarışıq karboksillədir və ya malate (MAL) və asetil-Koa üçün oksidativ dekarboksilasyon deyil (Jeoung et al., 1982; Magnusson et al., 2012; Merritt və s., 1991). Qaraciyərdə glyukoza və pyruvat asetil-Koa piruvatın dekarboksillənməsi maksimal səviyyədə olmasına baxmayaraq, ketogenezə əhəmiyyətsiz dərəcədə kömək edir (Jeoung və s., 2011).
Acetyl-CoA terminal oksidləşmə yolu ilə ATP nəslindən kənarda hepatik vasitə vasitə metabolizmasının tərkibində bir neçə rol oynayır (həmçinin, keton vücud metabolizmasının, post-translational modifikasiyasının və hüceyrə fiziologiyasının inteqrasiyası bax). Acetyl-CoA allosterik olaraq (i) pyruvate carboxylase (PC) aktivləşdirir və beləliklə, metabolitlərin TCA dövrü (Owen və s., 2002; Scrutton və Utter, 1967) daxil anaplerotik girişini artıran metabolik nəzarət mexanizmini aktivləşdirir və (ii) pyruvat dehidrogenaz (Cooper və ark., 1975) pirofiltratı və pyruvatı dehidrogenazın (PDH) inhibe edən kinaz, bununla da pyruvatın anapleroz vasitəsilə TCA dövrünə axını artırır. Bundan əlavə, mitokondriyal asetil-CoA-nı nəql edilə bilən metabolitlərə çevirən mexanizmlər vasitəsilə artırılmış sitoplazmik asetil-CoA yağ asiti oksidləşməsini maneə törədir: asetil-KoA karboksilaz (ACC) asetil-Koa malonil-Koa-yə çevrilməsi, lipogen substrat və mitokondrial CPT1 allosterik inhibitoru [Kahn et al., 2005; McGarry və Foster, 1980]. Beləliklə, mitokondriyal asetil-CoA hovuzu hemoglobin vasitə metabolizmasının əsas aspektlərini təşkil edən ketogenezin yayılması yolu ilə tənzimlənir və tənzimlənir.
Keton orqanlarının qeyri-oksidativ metabolik tərifləri
Qaraciyərdən çıxan ketonların başlıca taleyi SCOT-asılı extrahepatik oksidləşmədir. AcAc, mitokondriyadan ixrac edilə və sitoplazmik asetoasetil-KoA sintetazla (AACS, Şəkil 1B) katalizlənmiş ATP-qarışıq reaksiya ilə AcAc-CoA-a çevrilməsi yolu ilə anabolik yollarla istifadə edilə bilər. Bu yol beyin inkişafında və laktasiyalı məmə bezi zamanı aktivdir (Morris, 2005, Robinson və Williamson, 1978; Ohgami və s., 2003). AACS də yağlı toxuma ilə yüksək ifadə olunur və osteoklastları aktivləşdirir (Aguilo və s., 2010; Yamasaki et al., 2016). Sitoplazmik AcAc-CoA ya sterol biosentezinə qarşı sitosolik HMGCS1 tərəfindən yönəldilə bilər və ya malonil-Koa qədər karboksillənmiş asetil-Koa (ACAA1 və ACAT2) iki sitoplazmik tiolazdan birinə bölünür və yağ turşularının sintezinə kömək edir (Bergstrom et Edmund, 1984; Endemann et al., 1974; Geelen və digərləri, 1982, Webber və Edmond, 1983).
Fizioloji əhəmiyyəti hələ müəyyən edilməsə də, ketonlar qaraciyərdə belə anabolik substrat kimi xidmət edə bilər. Süni eksperimental kontekstlərdə AcAc yeni sintez edilmiş lipidlərin yarısına və yeni sintez edilmiş xolesterolun 75%-ə qədərinə töhfə verə bilər (Endemann və digərləri, 1982; Geelen və digərləri, 1983; Freed və digərləri, 1988). AcAc qaraciyər yağının natamam oksidləşməsindən əmələ gəldiyi üçün AcAc-ın in vivo lipogenezdə iştirak etmək qabiliyyəti qaraciyərin boş dövriyyəsini nəzərdə tutur, burada yağdan əldə edilən ketonlardan lipid istehsalı üçün istifadə oluna bilər, bu anlayış fizioloji əhəmiyyəti eksperimental yoxlama tələb edir. adaptiv və ya uyğun olmayan rollar (Solinas et al., 2015). AcAc xolesterogenezi həvəslə təmin edir, aşağı AACS Km-AcAc (~50 μM) hətta qidalanmış vəziyyətdə belə AcAc aktivləşməsinə üstünlük verir (Bergstrom və digərləri, 1984). Sitoplazmik keton metabolizminin dinamik rolu siçanların birincili embrion neyronlarında və 3T3-L1 törəmə-adipositlərində təklif edilmişdir, çünki AACS yıxılması hər bir hüceyrə növünün differensiasiyasını pozmuşdur (Hasegawa et al., 2012a; Hasegawa et al., 2012b). In vivo siçanlarda AACS-nin yıxılması serum xolesterolunu azaldır (Hasegawa et al., 2012c). SREBP-2, xolesterin biosintezinin master transkripsiya tənzimləyicisi və peroksizom proliferator aktivləşdirilmiş reseptor (PPAR)-? AACS transkripsiya aktivatorlarıdır və neyrit inkişafı zamanı və qaraciyərdə onun transkripsiyasını tənzimləyir (Aguilo et al., 2010; Hasegawa et al., 2012c). Birlikdə götürüldükdə, sitoplazmik keton cisimlərinin metabolizmi seçilmiş şəraitdə və ya xəstəliyin təbii tarixçələrində vacib ola bilər, lakin qaraciyərdən əldə edilən keton cisimlərinin xaric edilməsi üçün qeyri-adekvatdır, çünki funksiya mutasiyalarının itirilməsi ilə əsas oksidləşdirici taleyin selektiv pozulmasında kütləvi hiperketonemiya baş verir. SCOT-a (Berry et al., 2001; Cotter et al., 2011).
HMGCS2 və SCOT / OXCT1 tənzimlənməsi
Sitozolik HMGCS'yi kodlayan gen mitokondriyalının ayrılığı, omurilik inkişafında erkən dövrdə meydana gəldi və bədən çəkisi nisbətlərinə yüksək beyin olan qaraciyər ketogenezini dəstəkləməyə ehtiyac duyuldu (Boukaftane və s., 1994; Cunnane and Crawford, 2003). Təbii olaraq baş verən HMGCS2 mutasyonları, insanlarda hipoketotik hipoqlikemiya (Pitt et al., 2015; Thompson et al., 1997) yaralarına səbəb olur. Sağlam HMGCS2 ifadəsi hepatositlər və kolon epiteli ilə məhdudlaşır və onun ifadəsi və fermenti fəaliyyəti müxtəlif mexanizmlər vasitəsilə əlaqələndirilir (Mascaro və ark., 1995; McGarry və Foster, 1980; Robinson və Williamson, 1980). HMGCS2-ə təsir göstərən fizioloji dövlətlərin tam əhatə dairəsi daha çox izah edilməsini tələb edirsə də, onun ifadə və / və ya fəaliyyəti erkən postnatal dövrdə, yaşlanma, diabet, aclıq və ya ketogenic dietin yuyulması zamanı tənzimlənir (Balas və Fery, 1989; Cahill GF Jr, 2006 Girard və ark., 1992, Hegardt, 1999; Satapati və s., 2012; Sengupta və s., 2010). Döldə, Hmgcs5 geninin 2� qanad bölgəsinin metilasiyası onun transkripsiyası ilə tərs korrelyasiya olur və doğuşdan sonra qismən tərsinə çevrilir (Arias və digərləri, 1995; Ayte və digərləri, 1993; Ehara və digərləri, 2015; Ferre və başqaları. ., 1983). Eynilə, qaraciyər Bdh1 doğumdan süngəyə qədər artan bir inkişaf nümunəsi nümunəsi nümayiş etdirir və həmçinin bir fibroblast artım faktoru (FGF) -21-bağımlı bir şəkildə ketogenic diet (Badman və s., 2007; Zhang et al., 1989 ). Memelilərdə ketogenez həm insulin, həm də glukagona yüksək təsir göstərir, buna görə də təzyiq və stimullaşdırılır (McGarry və Foster, 1977). Insülin adipoz toxuması lipolizini bastırır, beləliklə, glukagon qaraciyərə birbaşa təsiri ilə ketogenic fluxı (Hegardt, 1999) artırarkən substratın ketogenezindən məhrum olur. Hmgcs2 transkripsiyası, insulin-fosfatidilinositol-2-kinaz / Akt vasitəsilə inhibe edilmiş və glucagon-cAMP-p3 sinyalizasiyası (Arias və ark., 300; Hegardt, 1995; Quant et al. , 1999; Thumelin et al., 1990; von Meyenn et al., 1993; Wolfrum et al., 2013; Wolfrum et al., 2004). PPAR? (Rodriguez və digərləri, 1994) hədəfi ilə birlikdə FGF21 (Badman et al., 2007) də aclıq və ya ketogenik pəhrizin tətbiqi zamanı qaraciyərdə Hmgcs2 transkripsiyasına səbəb olur (Badman et al., 2007; Inagaki et al., 2007). ). PPAR induksiyası? fetal fiziologiyadan neonatal fiziologiyaya keçiddən əvvəl baş verə bilər, FGF21 aktivasiyası isə histon deasetilaz (HDAC)-3-ün OHB vasitəçiliyi ilə inhibe edilməsi yolu ilə erkən neonatal dövrdə üstünlük təşkil edə bilər (Rando et al., 2016). mTORC1 (rapamisin kompleksinin məməli hədəfi 1) PPAR-ın asılı inhibisyonu? transkripsiya fəaliyyəti də Hmgcs2 gen ifadəsinin əsas tənzimləyicisidir (Sengupta və digərləri, 2010) və qaraciyər PER2, master sirkadiyalı osilator, dolayı yolla Hmgcs2 ifadəsini tənzimləyir (Chavan və digərləri, 2016). Son müşahidələr göstərir ki, ekstrahepatik şişin yaratdığı interleykin-6 PPAR vasitəsilə ketogenezi pozur? bastırma (Flint et al., 2016).
HMGCS2 enzim aktivliyi birdən çox PTM vasitəsilə tənzimlənir. HMGCS2 serin fosforilasyonu in vitro fəaliyyətini artırdı (Grimsrud və s., 2012). HMGCS2 aktivliyi succinyl-CoA və lizin qalıqlarının succinilasyonu ilə alllier olaraq inhibe edilmişdir (Arias və s., 1995; Hegardt, 1999; Lowe və Tubbs, 1985; Quant və digərləri, 1990, Rardin və s., 2013; Reed et al. 1975; Thumelin və digərləri, 1993). Hepatik mitokondriyada HMGCS2, HMGCL və BDH1 lizin qalıqlarının succinilasyonu NAD + asılı deasilaz sirtuin 5 (SIRT5) (Rardin və s., 2013) hədəfləridir. HMGCS2 aktivliyi SIRT3 lizin deasetilasiyası ilə də güclənir və asetiliya və suksinilasiya arasında qarışıqlıq HMGCS2 aktivliyini tənzimləyir (Rardin və s., 2013, Shimazu et al., 2013). Bu PTM-lərin HMGCS2 Km və Vmax-nı tənzimləmək qabiliyyətinə baxmayaraq, bu PTM-lərin dəyişməsi hələ də diqqətlə izlənilməmişdir və in vivo-da ketogenezin mexaniki mexanizmləri kimi təsdiqlənməmişdir.
SCOT hepatositlər istisna olmaqla, mitokondriyanı əhatə edən bütün memeli hüceyrələrində ifadə edilir. SCOT aktivliyinin və ketolizmanın əhəmiyyəti doğumdan sonra 48h-də (Cotter və s., 2011) hiperketonemik hipoqlikemiya səbəbindən vahid ölümü göstərən SCOT-KO farelerində göstərildi. Neyron və ya skelet miyositlərində SCOT toxuması xüsusi itkisi açlıq zamanı metabolik anormallikləri səbəb olur, lakin ölümcül deyil (Cotter və s., 2013b). İnsanlarda SCOT çatışmazlığı, ağır ketoacidosis ilə birlikdə erkən yaşlarda, letarji, qusma və komaya səbəb olur (Berry və s., 2001; Fukao və digərləri, 2000; Kassovska-Bratinova və digərləri, 1996; Niezen-Koning və s. , 1997, Saudubrey və digərləri, 1987, Snyderman və s., 1998, Tildon və Cornblath, 1972). SCOT gen və protein ifadə tənzimləyiciləri haqqında hücresel səviyyədə nisbətən çox azdır. Oxct1 mRNA ifadəsi və SCOT proteini və aktivliyi, ehtimal ki, PPAR-bağlı mexanizmlər (Fenselau və Wallis, 1974, Fenselau və Wallis, 1976, Grinblat və s., 1986; Okuda və s., 1991; Turko et al ., 2001; Wentz et al., 2010). Diabetik ketoasidozda qaraciyər ketogenezi və ekstrahepatik oksidləşmə arasındakı uyğunsuzluq SCOT aktivliyinin pozulması ilə daha da güclənir. Kardiyomiyositlərdə insulin-müstəqil qlükoza daşıyıcısının (GLUT1 / SLC2A1) aşkara çıxarılması da Oxct1 gen ifadəsini maneə törədir və qeyri-ketotik vəziyyətdə keton terminal oksidləşməsini azaldır (Yan və digərləri, 2009). Qaraciyərdə, Oxct1 mRNA bolluğu fetaldan neonatal dövrə (Thorrez və digərləri, 122) keçid zamanı aşkar olan mikroRNA-3 və histon methylation H27K3me2011 tərəfindən bastırılır. Lakin, postnatal dövrdə hepatik Oxct1 ifadəsinin basdırılması, əsasən Oxct1-ifadə edən hematopoietik progenitlərin qaraciyərdən çıxarılması ilə əlaqədardır, əvəzində mövcud olan Oxct1 ifadəsinin terminallaşmış fərqli hepatositlərdəki itkisi. Əslində, fərqli hepatositlərdə Oxct1 mRNA və SCOT proteininin ifadəsi olduqca aşağıdır (Orii və digərləri, 2008).
SCOT həmçinin PTM-lər tərəfindən tənzimlənir. Ferment, SIRT3 KO siçanlarının beyinlərində hiper-asetilləşmişdir ki, bu da AcAc-dan asılı asetil-CoA istehsalını azaldır (Dittenhafer-Reed et al., 2015). SCOT-nin tirozin qalıqlarının qeyri-enzimatik nitrasiyası da müxtəlif diabetik siçan modellərinin ürəklərində bildirilmiş fəaliyyətini zəiflədir (Marcondes və digərləri, 2001; Turko və digərləri, 2001; Wang və digərləri, 2010a). Bunun əksinə olaraq, triptofan qalıqlarının nitrasiyası SCOT fəaliyyətini artırır (Br�g�re et al., 2010; Rebrin et al., 2007). SCOT fəaliyyətini modulyasiya etmək üçün nəzərdə tutulmuş qalığa spesifik nitrasiya və ya de-nitrasiyanın molekulyar mexanizmləri mövcud ola bilər və izahat tələb edir.
Extrahepatic Ketogenezdə mübahisələr
Məməlilərdə əsas ketogen orqan qaraciyərdir və yalnız hepatositlər və bağırsaq epitel hüceyrələri HMGCS2-nin mitoxondrial izoformunu bol şəkildə ifadə edir (Cotter və digərləri, 2013a; Cotter və digərləri, 2014; McGarry və Foster, 1980; Robinson və Williamson, 1980, 1995) . Mürəkkəb polisaxaridlərin anaerob bakterial fermentasiyası nəticəsində məməlilərdə kolonositlər tərəfindən terminal oksidləşmə və ya ketogenez üçün udulan butirat əldə edilir (Cherbuy et al., 2016), kolonositlərin differensiasiyasında rol oynaya bilər (Wang et al., 2). Bağırsaq epitelial hüceyrələri və hepatositlər istisna olmaqla, HMGCS2014 demək olar ki, bütün digər məməli hüceyrələrində yoxdur, lakin şiş hüceyrələrində, mərkəzi sinir sisteminin astrositlərində, böyrəklərdə, pankreasda ekstrahepatik ketogenez perspektivi artır. hüceyrələrdə, retinal piqment epitelində (RPE) və hətta skelet əzələsində (Adijanto və s., 1992; Avogaro və digərləri, 2016; El Azzouny və digərləri, 2016; Grabacka və digərləri, 2015; Kang et al., 2014) ; Le Foll və digərləri, 2016; Nonaka və digərləri, 2016; Takagi və digərləri, 2016a; Thevenet və digərləri, 2011; Zhang və başqaları, 2). Ektopik HMGCS2016, xalis ketogenik qabiliyyəti olmayan toxumalarda müşahidə edilmişdir (Cook et al., 2010; Wentz et al., 2) və HMGCS2016, hüceyrə nüvəsi daxil olmaqla, perspektiv ketogenezdən asılı olmayan "ay işığı" fəaliyyətləri nümayiş etdirir (Chen et al. , 2010; Kostiuk et al., 1998; Meertens et al., XNUMX).
Keton cisimlərini oksidləşdirən hər hansı ekstrahepatik toxuma da HMGCS2 müstəqil mexanizmləri vasitəsilə keton cisimlərini toplamaq potensialına malikdir (Şəkil 2A). Bununla belə, keton cisimlərinin sabit vəziyyətdə olan konsentrasiyasının dövrandakından artıq olduğu heç bir ekstrahepatik toxuma yoxdur (Cotter və digərləri, 2011; Cotter və digərləri, 2013b; Harrison və Long, 1940), keton cisimlərinin aşağıya daşındığını vurğulayır. MCT1/2-dən asılı mexanizmlər vasitəsilə konsentrasiya qradiyenti. Görünən ekstrahepatik ketogenezin bir mexanizmi əslində keton oksidləşməsinin nisbi pozulmasını əks etdirə bilər. Əlavə potensial izahatlar keton cisimlərinin formalaşması sahəsinə aiddir. Birincisi, de novo ketogenez tiolaza və SCOT-un geri dönən enzimatik fəaliyyəti ilə baş verə bilər (Weidemann və Krebs, 1969). Asetil-KoA-nın konsentrasiyası nisbətən yüksək olduqda, normal olaraq AcAc oksidləşməsinə cavabdeh olan reaksiyalar tərs istiqamətdə işləyir (GOLDMAN, 1954). İkinci mexanizm ?-oksidləşmədən əldə edilən ara məhsullar TCA dövrünün darboğazına görə yığıldıqda baş verir, AcAc-CoA mitoxondrial 3-hidroksiasil-CoA dehidrogenaz və daha sonra 3-hidroksibutiril tərəfindən kataliz olunan reaksiya vasitəsilə l-?OHB-CoA-ya çevrilir. Kütləvi spektrometriya və ya rezonans spektroskopiyası ilə fizioloji enantiomer d-?OHB-dən fərqlənməyən l-?OHB-yə CoA deasilaza (Reed və Ozand, 1980). l-?OHB xromatoqrafik və ya enzimatik olaraq d-?OHB-dən fərqlənə bilər və ekstrahepatik toxumalarda mövcuddur, lakin qaraciyərdə və ya qanda yoxdur (Hsu et al., 2011). Hepatik ketogenez yalnız BDH substratı olan yeganə enantiomer olan d-?OHB istehsal edir (Ito və digərləri, 1984; Lincoln və digərləri, 1987; Reed və Ozand, 1980; Scofield və digərləri, 1982; Scofield və başqaları, 1982). Üçüncü HMGCS2-dən asılı olmayan mexanizm amin turşusu katabolizmi, xüsusən də leysin və lizin vasitəsilə d-?OHB yaradır. Dördüncü mexanizm yalnız aydındır, çünki o, etiketləmə artefaktına bağlıdır və buna görə də psevdoketogenez adlanır. Bu fenomen SCOT və tiolaza reaksiyalarının geri çevrilməsi ilə əlaqədardır və ekstrahepatik toxumada keton bədəni izləyicisinin izotopik seyreltilməsi səbəbindən keton cisimlərinin dövriyyəsinin həddindən artıq qiymətləndirilməsinə səbəb ola bilər (Des Rosiers və digərləri, 1990; Fink və digərləri, 1988) . Buna baxmayaraq, psevdoketogenez əksər kontekstlərdə əhəmiyyətsiz ola bilər (Bailey et al., 1990; Keller et al., 1978). Sxematik (Şəkil 2A) ketonların yüksək toxuma sabit konsentrasiyasını nəzərə alaraq tətbiq etmək üçün faydalı yanaşmanı göstərir.
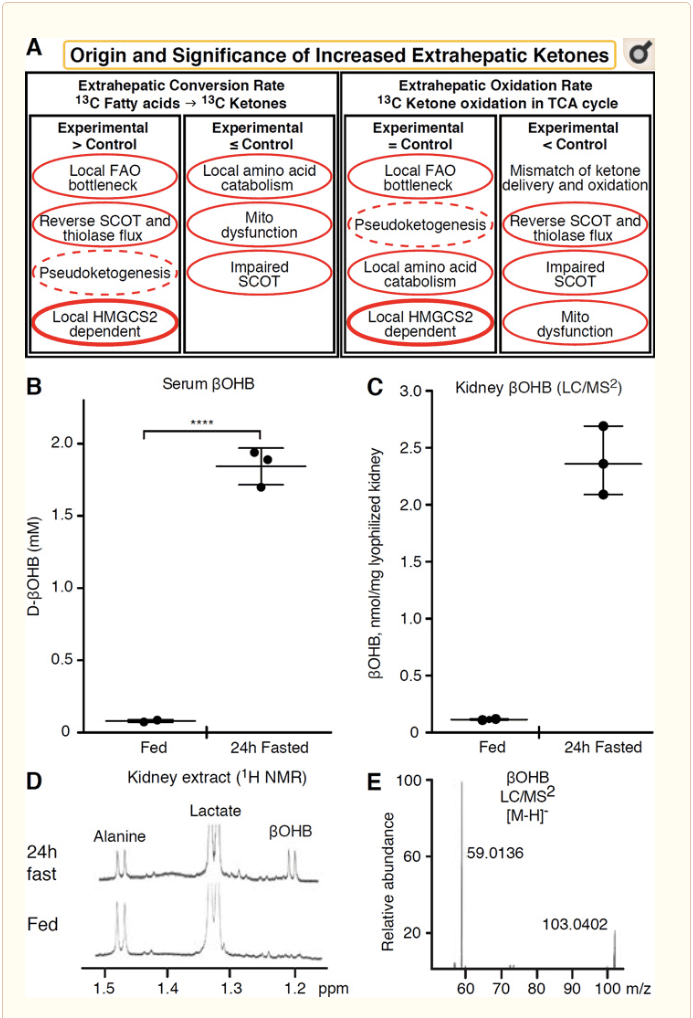

Böyrək son vaxtlar potensial ketogenik orqan kimi diqqət çəkir. Ştatların böyük əksəriyyətində böyrək qaraciyərdən əldə edilən keton cisimlərinin xalis istehlakçısıdır, keton cisimlərini qan axınından xaric edir və ya reabsorbsiya edir və böyrək ümumiyyətlə xalis keton cisimlərinin generatoru və ya konsentratoru deyildir (Robinson və Williamson, 1980). Klassik tədqiqatın müəllifləri süni eksperimental sistemdə ölçülən minimal böyrək ketogenezinin fizioloji cəhətdən əhəmiyyətli olmadığı qənaətinə gəldilər (Weidemann və Krebs, 1969). Bu yaxınlarda diabetik və otofagiya çatışmazlığı olan siçan modellərində böyrək ketogenezi haqqında nəticə çıxarıldı, lakin metabolik homeostazda çox orqan dəyişikliklərinin bir çox orqandakı girişlər vasitəsilə inteqrativ keton metabolizmasını dəyişdirməsi ehtimalı daha yüksəkdir (Takagi et al., 2016a; Takagi et al., 2016b; Zhang və başqaları, 2011). Son nəşrlərdən biri böyrək ketogenezini böyrəkdə işemiya-reperfuziya zədələnməsinə qarşı qoruyucu mexanizm kimi təklif etdi (Tran et al., 2016). Siçanların böyrək toxumasının ekstraktlarından ?OHB-nin mütləq tarazlıq konsentrasiyası ~4-12 mM səviyyəsində bildirildi. Bunun davamlı olub-olmadığını yoxlamaq üçün biz qidalanan və 24 saat ac qalan siçanlardan alınan böyrək ekstraktlarında ?OHB konsentrasiyalarının miqdarını təyin etdik. Serum ?OHB konsentrasiyaları 100 saatlıq aclıq zamanı ~2 μM-dən 24 mM-ə qədər artdı (Şəkil 2B), böyrək tarazlıq vəziyyətində ?OHB konsentrasiyaları qidalanma vəziyyətində təqribən 100 µM, 1 saat aclıqda isə yalnız 24 mM-ə çatdı (Şəkil 2). 45C�E), 1970 il əvvəl ölçülən konsentrasiyalara uyğun olan müşahidələr (Hems və Brosnan, 2014). Ketotik vəziyyətlərdə qaraciyərdən əldə edilən keton cisimlərinin renoprotektiv ola biləcəyi mümkündür, lakin böyrək ketogenezinin sübutu əlavə əsaslandırma tələb edir. Həqiqi ekstrahepatik ketogenezi dəstəkləyən inandırıcı sübutlar RPE-də təqdim edilmişdir (Adijanto et al., XNUMX). Bu maraqlı metabolik transformasiyanın RPE-dən əldə edilən ketonların fotoreseptorlara və ya Müller glia hüceyrələrinə axmasına imkan verməsi təklif edilmişdir ki, bu da fotoreseptorun xarici seqmentinin bərpasına kömək edə bilər.
Siqnal Vasitəçisi kimi ?OHB
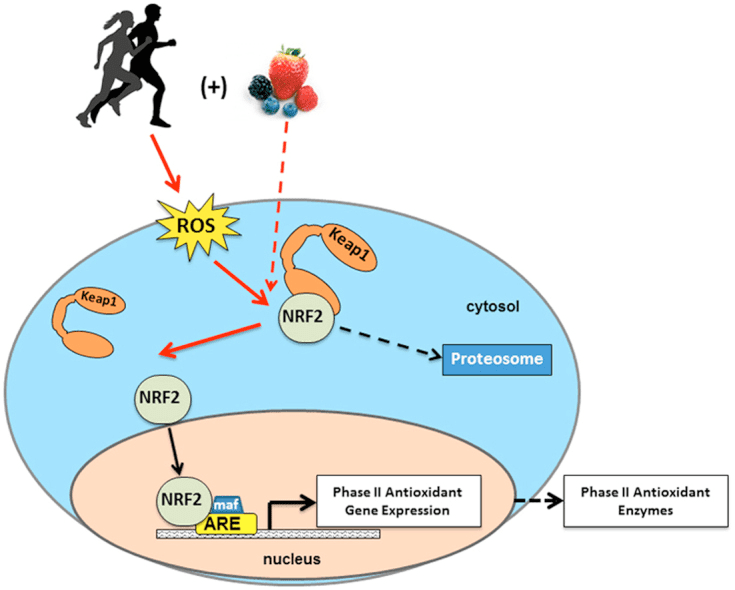
Enerji baxımından zəngin olsalar da, keton cisimləri hüceyrə homeostazında təxribatçı “qeyri-kanonik” siqnal rolunu oynayır (Şəkil 3) (Newman və Verdin, 2014; Rojas-Morales et al., 2016). Məsələn, ?OHB, histon asetilasiyasını artıran və bununla da oksidləşdirici stressi azaldan genlərin ifadəsini stimullaşdıran I sinif HDAC-ları inhibə edir (Shimazu et al., 2013). ?OHB özü oruc tutan və ya streptozotosinin səbəb olduğu diabetik siçanların qaraciyərlərindəki lizin qalıqlarında histon kovalent modifikatordur (Xie və digərləri, 2016) (həmçinin aşağıya baxın, Keton bədən metabolizmasının inteqrasiyası, translasiyadan sonrakı modifikasiya və hüceyrə fiziologiyası və Keton cisimləri, oksidləşdirici stress və neyroproteksiya).
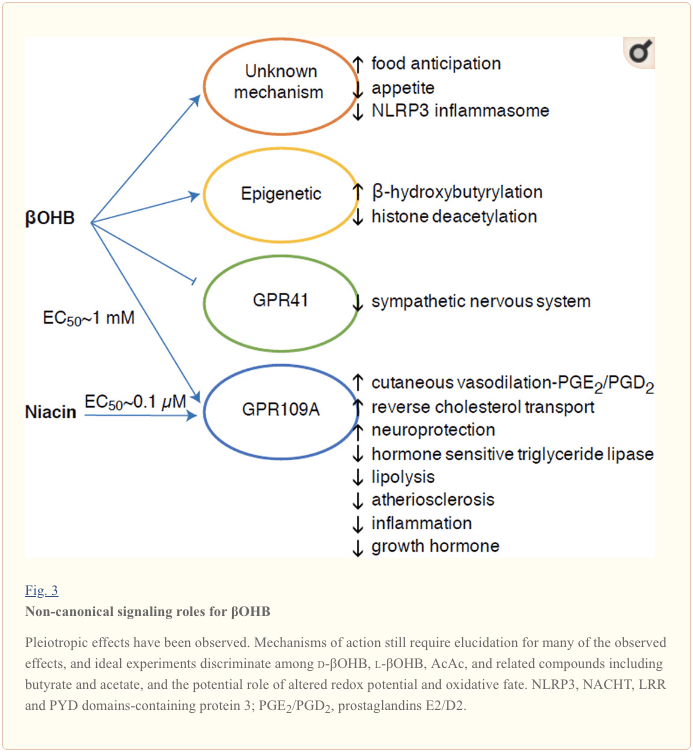
?OHB həm də G-proteinlə əlaqəli reseptorlar vasitəsilə effektordur. Aydın olmayan molekulyar mexanizmlər vasitəsilə simpatik sinir sisteminin fəaliyyətini boğur və G zülalı ilə əlaqəli reseptor 41 (GPR41) vasitəsilə qısa zəncirli yağ turşusu siqnalını maneə törətməklə ümumi enerji xərclərini və ürək dərəcəsini azaldır (Kimura və digərləri, 2011). OHB-nin ən çox öyrənilmiş siqnal təsirlərindən biri yağ toxumalarında (ağ və qəhvəyi) ifadə olunan hidrokarboksilik turşu GPCR alt ailəsinin üzvü olan GPR109A (həmçinin HCAR2 kimi tanınır) vasitəsilə baş verir (Tunaru et al., 2003) və immun hüceyrələri (Ahmed et al., 2009). ?OHB, AcAc deyil, d-?OHB, l-?OHB və butirat tərəfindən aktivləşdirilmiş GPR109A reseptorunun (EC50 ~770 �M) yeganə məlum endogen liqandıdır (Taggart et al., 2005). GPR109A-nın aktivləşdirilməsi üçün yüksək konsentrasiya həddi ketogenik pəhrizə riayət etməklə, aclıq və ya ketoasidoz zamanı əldə edilir ki, bu da yağ toxumasının lipolizinin inhibə edilməsinə gətirib çıxarır. GPR109A-nın anti-lipolitik təsiri adenilil siklazın inhibe edilməsi və cAMP-nin azalması, hormona həssas trigliserid lipazı inhibə etməklə davam edir (Ahmed et al., 2009; Tunaru et al., 2003). Bu, ketozun adipositlərdən esterləşdirilməmiş yağ turşularının sərbəst buraxılmasını azaltmaqla ketogenezə modulyator əyləc qoyduğu mənfi rəy dövrəsi yaradır (Ahmed və digərləri, 2009; Taggart et al., 2005), bu təsirin qarşısı alına bilər. lipolizi stimullaşdıran simpatik sürücü. Niacin (vitamin B3, nikotinik turşu) GRP50A üçün güclü (EC0.1 ~ 109 μM) liqanddır, dislipidemiyalar üçün onilliklər ərzində effektiv şəkildə istifadə olunur (Benyo və digərləri, 2005; Benyo və digərləri, 2006; Fabbrini və digərləri, 2010). Lukasova və başqaları, 2011; Tunaru və başqaları, 2003). Niasin makrofaqlarda tərs xolesterol daşınmasını gücləndirsə və aterosklerotik lezyonları azaltsa da (Lukasova və digərləri, 2011), OHB-nin aterosklerotik lezyonlara təsiri naməlum olaraq qalır. Baxmayaraq ki, GPR109A reseptoru qoruyucu rol oynayır və insult və neyrodegenerativ xəstəliklərdə ketogenik pəhriz istifadəsi arasında maraqlı əlaqələr mövcuddur (Fu və digərləri, 2015; Rahman və digərləri, 2014), GPR109A vasitəsilə ?OHB-nin qoruyucu rolu in vivo nümayiş etdirilməmişdir. .
Nəhayət, ?OHB iştaha və toxluğa təsir göstərə bilər. Ketogenik və çox aşağı enerji pəhrizlərinin təsirlərini ölçən tədqiqatların meta-analizi belə nəticəyə gəldi ki, bu pəhrizləri istehlak edən iştirakçılar nəzarət pəhrizləri ilə müqayisədə daha yüksək toxluq hissi nümayiş etdirirlər (Gibson et al., 2015). Bununla belə, bu təsirin ağlabatan izahı iştahı dəyişdirə biləcək əlavə metabolik və ya hormonal elementlərdir. Məsələn, gəmirici ketogenik pəhrizdə saxlanılan siçanlar, oxşar kalori qəbuluna baxmayaraq, qidalanma ilə qidalanan siçanlarla müqayisədə artan enerji xərcləri nümayiş etdirdi və dövran edən leptin və ya qidalanma davranışını tənzimləyən peptidlərin genləri dəyişdirilmədi (Kennedy et al., 2007). ?OHB tərəfindən iştahın yatırılmasını təklif edən təklif olunan mexanizmlər arasında həm siqnal, həm də oksidləşmə daxildir (Laeger et al., 2010). Sirkadiyalı ritm geninin (Per2) və xromatinin immunoprecipitation tədqiqatlarının hepatositlərə xas şəkildə silinməsi PER2-nin birbaşa Cpt1a genini aktivləşdirdiyini və dolayı yolla Hmgcs2-ni tənzimlədiyini, Per2 nokaut siçanlarında pozulmuş ketoza səbəb olduğunu ortaya qoydu (Chavan et al.,). Bu siçanlar sistemli ?OHB administrasiyası ilə qismən bərpa edilən zəif qida gözləntilərini nümayiş etdirdilər. Mərkəzi sinir sistemini birbaşa ?OHB hədəfi kimi təsdiqləmək və müşahidə olunan təsirlər üçün keton oksidləşməsinin lazım olub-olmadığını və ya başqa bir siqnal mexanizminin iştirak edib-etmədiyini təsdiqləmək üçün gələcək tədqiqatlara ehtiyac olacaq. Digər tədqiqatçılar qida qəbulunun tənzimləyicisi kimi ventromedial hipotalamusda yerli astrositdən qaynaqlanan ketogenezin mümkünlüyünə istinad etdilər, lakin bu ilkin müşahidələr genetik və sel əsaslı qiymətləndirmələrdən də faydalanacaq (Le Foll et al., 2016). Ketoz və qida çatışmazlığı arasındakı əlaqə maraq doğurur, çünki aclıq və toxluq uğursuz arıqlama cəhdlərində vacib elementlərdir.
Keton bədən metabolizmasının, post-Translational modifikasiyasının və hüceyrə fiziologiyasının inteqrasiyası
Keton orqanları, hücresel metabolizma (Pietrocola ve arkadaşları, 2015) içinde görülen rolleri sergileyen bir ara ara ürün olan asetil-CoA'nın bölünmüş hovuzlarına yardım edir. Acetyl-CoA'nın bir roli asetilasyon üçün enzimatik katalizli bir histon kovalent modifikasiyası üçün substrat kimi xidmət etməkdir (Choudhary et al., 2014; Dutta və s., 2016; Fan et al., 2015; Menzies et al., 2016 ). Çoxlarının qeyri-enzimatik mexanizmlər vasitəsilə meydana gələ biləcəyi dinamik olaraq asetillenmiş mitokondriyal zülallar da hesablama proteomikası tədqiqatlarından (Dittenhafer-Reed və s., 2015; Hebert et al., 2013; Rardin və s., 2013 , Shimazu et al., 2010). Lizin deasetilazları sintez substrat (Sirtuins, SIRTs) kimi bir sink kofaktoru (məsələn, nükleositozolik HDAC) və ya NAD + istifadə edirlər (Choudhary və s., 2014; Menzies et al., 2016). Asetilproteom, asetil-koa hövzəsinin hər iki sensoru və effektoru kimi fəaliyyət göstərir, fizioloji və genetik maneə kimi hər bir nəticəni asetiliyanın qeyri-enzimatik qlobal dəyişmələrində (Weinert və s., 2014). Hüceyrə metabolitləri lizin qalıqları asetiliyəsinin modulatorları kimi xidmət edərkən, bolluğu çox dinamik olan keton orqanlarının rolunu nəzərə almaq vacibdir.
?OHB ən azı iki mexanizm vasitəsilə epigenetik dəyişdiricidir. Oruc, kalori məhdudlaşdırması, birbaşa administrasiya və ya uzun müddətli məşq nəticəsində yaranan artan OHB səviyyələri HDAC inhibisyonunu və ya histon asetiltransferaza aktivləşməsini (Marosi və digərləri, 2016; Sleiman və digərləri, 2016) və ya oksidləşdirici stresə (Shimazu və digərləri, 2013) səbəb olur. . HDAC3-ün OHB inhibisyonu yeni doğulmuş metabolik fiziologiyanı tənzimləyə bilər (Rando et al., 2016). Müstəqil olaraq, ?OHB özü birbaşa histon lizin qalıqlarını dəyişdirir (Xie et al., 2016). Uzun müddətli oruc tutma və ya steptozotosinin səbəb olduğu diabetik ketoasidoz histonun ?-hidroksibutirilasiyasını artırdı. Lizin ?-hidroksibutirilasiya və asetilləşmə sahələrinin sayı müqayisə oluna bilsə də, asetilləşmədən stoxiometrically daha çox histon ?-hidroksibutirilasiya müşahidə edildi. Fərqli genlərə histon lizin ?-hidroksibutirilasiya, asetilləşmə və ya metilləşmə ilə müqayisədə fərqli hüceyrə funksiyaları təklif edildi. ?-hidroksibutirilasiyanın kortəbii və ya fermentativ olması məlum deyil, lakin keton cisimləri vasitəsilə transkripsiyaya dinamik təsir göstərən mexanizmlərin diapazonunu genişləndirir.
Kalori məhdudiyyəti və qida çatışmazlığı zamanı əsas hüceyrə yenidən proqramlaşdırma hadisələri, qaraciyər və ekstrahepatik toxumalarda posttranslational səviyyədə ketogenik və ketolitik zülalları tənzimləyən müvafiq olaraq SIRT3 və SIRT5-dən asılı mitoxondrial deasetilasiya və desuksinilləşmədə vasitəçilik edilə bilər (Dittenfer s. 2015; Hebert və başqaları, 2013; Rardin və başqaları, 2013; Shimazu və başqaları, 2010). İşğal edilmiş ərazilərin stoxiometrik müqayisəsi mütləq metabolik axının dəyişməsi ilə birbaşa əlaqəli olmasa da, mitoxondrial asetilləşmə dinamikdir və fermentativ asetiltransferazalardan çox asetil-KoA konsentrasiyası və ya mitoxondrial pH tərəfindən idarə oluna bilər (Wagner və Payne, 2013). SIRT3 və SIRT5-in keton cisimlərini metabolizə edən fermentlərin fəaliyyətini modulyasiya etməsi ketonların asetilproteom, suksinilproteom və digər dinamik hüceyrə hədəflərinin formalaşmasında qarşılıqlı rolu sualını doğurur. Həqiqətən, ketogenezin variasiyaları NAD+ konsentrasiyalarını əks etdirdiyi üçün keton istehsalı və bolluğu sirtuin fəaliyyətini tənzimləyə bilər və bununla da ümumi asetil-KoA/süksinil-KoA hovuzlarına, asilproteomuna və beləliklə, mitoxondrial və hüceyrə fiziologiyasına təsir göstərə bilər. Ferment lizin qalıqlarının ?-hidroksibutirilasiyası hüceyrənin yenidən proqramlaşdırılmasına daha bir qat əlavə edə bilər. Ekstrahepatik toxumalarda keton cisimlərinin oksidləşməsi hüceyrə homeostazında analoji dəyişiklikləri stimullaşdıra bilər. Asetil-KoA hovuzlarının bölmələri yüksək səviyyədə tənzimlənsə və geniş spektrli hüceyrə dəyişikliklərini əlaqələndirsə də, keton cisimlərinin həm mitoxondrial, həm də sitoplazmik asetil-KoA konsentrasiyalarını birbaşa formalaşdırmaq qabiliyyəti aydınlaşdırma tələb edir (Chen et al., 2012; Corbet et al., 2016; Pouqovkina və başqaları, 2014; Schwer və başqaları, 2009; Wellen və Tompson, 2012). Asetil-KoA konsentrasiyaları ciddi şəkildə tənzimləndiyinə və asetil-KoA membran keçirmədiyinə görə asetil-KoA homeostazını koordinasiya edən sürücü mexanizmləri, o cümlədən TCA dövründə istehsal və terminal oksidləşmə, keton cisimlərinə çevrilmə, mitoxondrial prosesləri nəzərə almaq çox vacibdir. karnitin asetiltransferaza (CrAT) vasitəsilə axıdılması və ya sitrata çevrildikdən sonra asetil-KoA-nın sitozola ixracı və ATP sitrat liazası (ACLY) ilə sərbəst buraxılması. Hüceyrə asetilproteomunda və homeostazda bu sonuncu mexanizmlərin əsas rolları ketogenez və keton oksidləşməsinin rollarının uyğun şəkildə başa düşülməsini tələb edir (Das və digərləri, 2015; McDonnell və digərləri, 2016; Moussaieff və digərləri, 2015; Overmyer et al., 2015; Seiler et al., 2014; Seiler et al., 2015; Wellen et al., 2009; Wellen and Thompson, 2012). Məqsədləri və nəticələri müəyyən etmək üçün genetik cəhətdən manipulyasiya edilmiş modellərin qurulmasında metabolomika və asilproteomikada konvergent texnologiyalar tələb olunacaq.
Keton orqanlarına qarşı anti-və iltihablı cavablar
Ketoz və keton cisimləri iltihabı və immun hüceyrə funksiyasını modulyasiya edir, lakin müxtəlif və hətta uyğunsuz mexanizmlər təklif edilmişdir. Uzun müddətli qida çatışmazlığı iltihabı azaldır (Youm və digərləri, 2015), lakin 1-ci tip diabetin xroniki ketozu iltihab əleyhinə bir vəziyyətdir (Jain və digərləri, 2002; Kanikarla-Marie və Jain, 2015; Kurepa et al., 2012). ). İltihabda ?OHB üçün mexanizm əsaslı siqnal rolları ortaya çıxır, çünki makrofaqlar və ya monositlər də daxil olmaqla bir çox immun sistemi hüceyrələri GPR109A-nı bol şəkildə ifadə edir. ?OHB əsasən antiinflamatuar reaksiya göstərsə də (Fu et al., 2014; Gambhir et al., 2012; Rahman et al., 2014; Youm et al., 2015), keton cisimlərinin yüksək konsentrasiyası, xüsusən də AcAc, pro-iltihab reaksiyasını tetikler (Jain və digərləri, 2002; Kanikarla-Marie və Jain, 2015; Kurepa və digərləri, 2012).
GPR109A liqandlarının ateroskleroz, piylənmə, iltihablı bağırsaq xəstəliyi, nevroloji xəstəlik və xərçəngdə antiinflamatuar rolları nəzərdən keçirilmişdir (Graff et al., 2016). GPR109A ifadəsi diabetik modellərin RPE hüceyrələrində, insan diabetik xəstələrdə (Gambhir və digərləri, 2012) və neyrodejenerasiya zamanı mikrogliyada artırılır (Fu və digərləri, 2014). ?OHB-nin antiinflamatuar təsiri RPE hüceyrələrində GPR109A həddindən artıq ifadəsi ilə gücləndirilir və farmakoloji inhibə və ya GPR109A-nın genetik nokautu ilə ləğv edilir (Gambhir et al., 2012). ?OHB və ekzogen nikotinik turşu (Taggart et al., 2005), hər ikisi TNF-də antiinflamatuar təsir göstərir? və ya qismən NF-ni inhibə edərək proinflamatuar zülalların (iNOS, COX-2) və ya ifraz olunan sitokinlərin (TNF?, IL-1?, IL-6, CCL2/MCP-1) səviyyələrini azaltmaqla LPS-induksiya etdiyi iltihab. -?B translokasiyası (Fu et al., 2014; Gambhir et al., 2012). ?OHB ER stressini və NLRP3 iltihabını azaldır, antioksidant stres cavabını aktivləşdirir (Bae və digərləri, 2016; Youm və digərləri, 2015). Bununla belə, neyrodegenerativ iltihabda GPR109A-dan asılı olan OHB vasitəçiliyi ilə qorunma MAPK yol siqnalı (məsələn, ERK, JNK, p38) kimi iltihab vasitəçilərini əhatə etmir (Fu və digərləri, 2014), lakin COX-1-dən asılı PGD2 tələb edə bilər. istehsalı (Rahman et al., 2014). Maraqlıdır ki, işemik insult modelində neyroprotektiv təsir göstərmək üçün GPR109A makrofaq tələb olunur (Rahman və digərləri, 2014), lakin OHB-nin sümük iliyindən törəmə makrofaqlarda NLRP3 iltihabını inhibə etmək qabiliyyəti GPR109A-dan müstəqildir (Youm et al. ., 2015). Əksər tədqiqatlar ?OHB-ni antiinflamatuar təsirlərlə əlaqələndirsə də, ?OHB pro-iltihablı ola bilər və dana hepatositlərində lipid peroksidləşməsinin markerlərini artırır (Shi et al., 2014). Beləliklə, ?OHB-nin anti-iltihab əleyhinə təsirləri hüceyrə növündən, ?OHB konsentrasiyasından, məruz qalma müddətindən və ko-modulyatorların mövcudluğundan və ya olmamasından asılı ola bilər.
?OHB-dən fərqli olaraq, AcAc pro-iltihab siqnalını aktivləşdirə bilər. Yüksək AcAc, xüsusilə yüksək qlükoza konsentrasiyası ilə, bir NADPH oksidaz / oksidləşdirici stressdən asılı mexanizm vasitəsilə endotel hüceyrələrinin zədələnməsini gücləndirir (Kanikarla-Marie və Jain, 2015). Diabetik anaların göbək kordonunda yüksək AcAc konsentrasiyası daha yüksək protein oksidləşmə sürəti və MCP-1 konsentrasiyası ilə əlaqələndirildi (Kurepa et al., 2012). Diabetik xəstələrdə yüksək AcAc TNF ilə əlaqələndirilirmi? ifadəsi (Jain və digərləri, 2002) və AcAc, lakin ?OHB deyil, TNF-nin səbəb olduğu, MCP-1 ifadəsi, ROS yığılması və U937 insan monosit hüceyrələrində cAMP səviyyəsinin azalması (Jain və digərləri, 2002; Kurepa və s. ., 2012).
Keton bədənindən asılı siqnal hadisələri tez-tez yalnız yüksək keton bədən konsentrasiyaları (> 5 mM) ilə və aydın olmayan mexanizmlər vasitəsilə ketonları pro- və ya antiinflamatuar təsirlərlə əlaqələndirən bir çox tədqiqat halında tetiklenir. Bundan əlavə, ?OHB-nin AcAc-ə qarşı iltihaba zidd təsirləri və AcAc/?OHB nisbətinin mitoxondrial redoks potensialına təsir etmək qabiliyyətinə görə, keton cisimlərinin hüceyrə fenotiplərində rolunu qiymətləndirən ən yaxşı təcrübələr AcAc və ? OHB müxtəlif nisbətlərdə və müxtəlif məcmu konsentrasiyalarda [məsələn, (Saito et al., 2016)]. Nəhayət, AcAc kommersiya olaraq yalnız litium duzu və ya istifadə etməzdən əvvəl əsas hidroliz tələb edən etil ester kimi alına bilər. Litium kation müstəqil olaraq siqnal ötürülməsi kaskadlarını induksiya edir (Manji et al., 1995), AcAc anion isə labildir. Nəhayət, rasemik d/l-?OHB-dən istifadə edilən tədqiqatlar çaşdırıla bilər, çünki yalnız d-?OHB stereoizomeri AcAc-ə oksidləşə bilər, lakin d-?OHB və l-?OHB hər biri GPR109A vasitəsilə siqnal verə bilər, NLRP3 iltihabını inhibə edə bilər, və lipogenik substrat kimi xidmət edir.
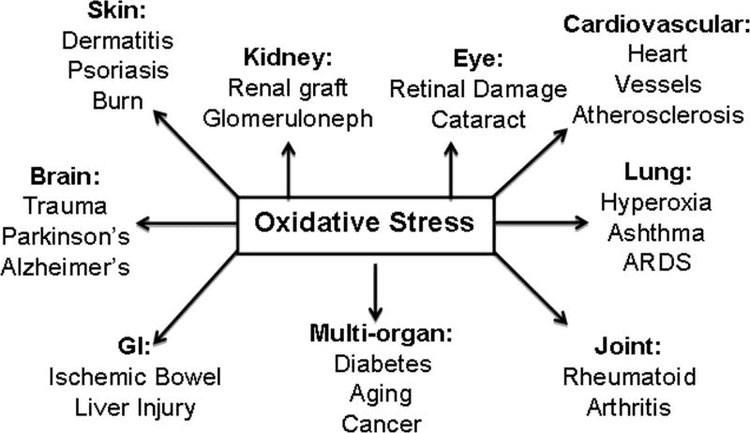
Keton cisimləri, oksidativ stress və neyrotropiya
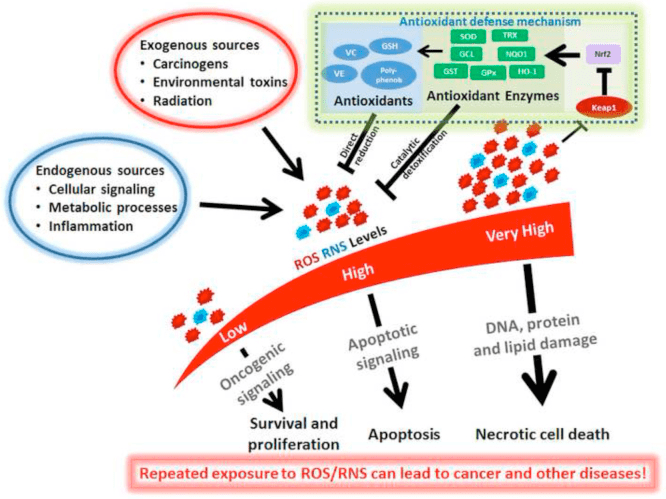
Oksidləşdirici stress, adətən, həddindən artıq istehsal və/və ya xaric edilmənin pozulması səbəbindən ROS-un həddindən artıq şəkildə təqdim olunduğu bir vəziyyət kimi müəyyən edilir. Keton cisimlərinin antioksidant və oksidləşdirici stressi yumşaldıcı rolları həm in vitro, həm də in vivo, xüsusən də neyroproteksiya kontekstində geniş şəkildə təsvir edilmişdir. Əksər neyronlar yağ turşularından effektiv şəkildə yüksək enerjili fosfatlar yaratmadığından, lakin karbohidratlar çatışmazlığı olanda keton cisimlərini oksidləşdirdiyindən, keton cisimlərinin neyroprotektiv təsiri xüsusilə vacibdir (Cahill GF Jr, 2006; Edmond et al., 1987; Yang). və başqaları, 1987). Oksidləşdirici stress modellərində, BDH1 induksiyası və SCOT-un bastırılması, keton bədən metabolizminin müxtəlif hüceyrə siqnallarını, redoks potensialını və ya metabolik tələbləri təmin etmək üçün yenidən proqramlaşdırıla biləcəyini təklif edir (Nagao və digərləri, 2016; Tieu və digərləri, 2003).
Keton cisimləri neyronlarda və kardiyomiyositlərdə hüceyrə zədələnməsi, zədə, ölüm və aşağı apoptoz dərəcələrini azaldır (Haces və s., 2008; Maalouf və digərləri, 2007; Nagao və digərləri, 2016; Tieu və digərləri, 2003). Çağırılan mexanizmlər müxtəlifdir və həmişə konsentrasiya ilə xətti əlaqəli deyil. (d və ya l)-?OHB-nin aşağı millimolyar konsentrasiyası ROS-u (hidroksil anionu) təmizləyir, AcAc isə çoxsaylı ROS növlərini təmizləyir, lakin yalnız fizioloji diapazonu (IC50 20-67 mM) aşan konsentrasiyalarda (Haces et al., 2008) . Əksinə, elektron nəqli zəncirinin redoks potensialına faydalı təsir adətən d-?OHB ilə əlaqəli bir mexanizmdir. Hər üç keton cismi (d/l-?OHB və AcAc) neyron hüceyrələrinin ölümünü və qlikolizin kimyəvi inhibəsi ilə tetiklenen ROS yığılmasını azaltsa da, yalnız d-?OHB və AcAc neyron ATP azalmasının qarşısını aldı. Əksinə, hipoqlikemik in vivo modeldə (d və ya l)-?OHB, lakin AcAc deyil, hipokampal lipid peroksidləşməsinin qarşısını aldı (Haces və digərləri, 2008; Maalouf və digərləri, 2007; Marosi və digərləri, 2016; Murphy, 2009). ; Tieu və başqaları, 2003). Ketogenik pəhriz (87% kkal yağ və 13% protein) ilə qidalanan siçanların in vivo tədqiqatları antioksidan gücün neyroanatomik variasiyasını nümayiş etdirdi (Ziegler və digərləri, 2003), burada ən dərin dəyişikliklər hipokampusda müşahidə edildi, glutatyon peroksidaz və ümumi artımla. antioksidant imkanlar.
Ketogenik pəhriz, keton esterləri (həmçinin ketogenik pəhriz və ekzogen keton cisimlərinin terapevtik istifadəsinə baxın) və ya OHB administrasiyası işemik insult modellərində neyroproteksiyaya malikdir (Rahman et al., 2014); Parkinson xəstəliyi (Tieu və digərləri, 2003); mərkəzi sinir sistemi oksigen toksiklik nöbet (D'Agostino et al., 2013); epileptik spazmlar (Yum et al., 2015); mitoxondrial ensefalomiopatiya, laktik asidoz və vuruşa bənzər (MELAS) epizodları sindromu (Frey və digərləri, 2016) və Alzheimer xəstəliyi (Cunnane və Crawford, 2003; Yin və digərləri, 2016). Əksinə, son hesabat, mitoxondrial biogenez və antioksidan imzaların artmasına baxmayaraq, anormal mitoxondrial DNT təmirinin transgenik siçan modelində ketogenik pəhriz tərəfindən neyrodegenerativ irəliləmənin histopatoloji sübutunu nümayiş etdirdi (Lauritzen et al., 2016). Digər ziddiyyətli hesabatlar yüksək keton bədən konsentrasiyalarına məruz qalmanın oksidləşdirici stresə səbəb olduğunu göstərir. Yüksək ?OHB və ya AcAc dozaları dana hepatositlərində azot oksidinin ifrazını, lipidlərin peroksidləşməsini, SOD, glutatyon peroksidaz və katalazın ekspressiyasını azaldır, siçovul hepatositlərində isə MAPK yolunun induksiyası AcAc-ə aid edilir, lakin ?OHB deyil (Abdelmegeed (Abdelmegeed). ; Shi et al., 2004; Shi et al., 2014).
Birlikdə götürdükdə, əksər hesabatlar OHB-ni oksidləşdirici stressin zəifləməsi ilə əlaqələndirir, çünki onun tətbiqi ROS/superoksid istehsalını maneə törədir, lipid peroksidləşməsi və zülal oksidləşməsinin qarşısını alır, antioksidant protein səviyyələrini artırır və mitoxondrial tənəffüsü və ATP istehsalını yaxşılaşdırır (Abdelmegeed et al., 2004; Haces və başqaları, 2008; Jain və başqaları, 1998; Jain və başqaları, 2002; Kanikarla-Marie və Jain, 2015; Maalouf və digərləri, 2007; Maalouf və Rho, 2008; Marosi və digərləri, 2016;eu və başqaları, 2003; Yin və başqaları, 2016; Ziegler və başqaları, 2003). AcAc oksidləşdirici stresin induksiyası ilə OHB-dən daha birbaşa əlaqəli olsa da, bu təsirlər həmişə prospektiv iltihab əleyhinə reaksiyalardan asanlıqla ayrılmır (Jain və digərləri, 2002; Kanikarla-Marie və Jain, 2015; Kanikarla-Marie və Jain, 2016). Bundan əlavə, nəzərə almaq vacibdir ki, pleiotropik ketogenik diyetlərin verdiyi açıq-aydın antioksidant fayda keton cisimlərinin özləri tərəfindən ötürülə bilməz və keton cisimləri tərəfindən verilən neyroqoruma tamamilə oksidləşdirici stresə aid edilə bilməz. Məsələn, qlükoza məhrumiyyəti zamanı, kortikal neyronlarda qlükoza məhrumiyyəti modelində ?OHB otofagik axını stimullaşdırdı və neyron ölümün azalması ilə əlaqəli olan autofaqosom yığılmasının qarşısını aldı (Camberos-Luna et al., 2016). d-?OHB həmçinin kanonik antioksidant zülalları FOXO3a, SOD, MnSOD və katalazı, HDAC inhibisyonu yolu ilə induksiya edir (Nagao et al., 2016; Shimazu et al., 2013).
Qeyri-Alkoqollu Yağlı Qaraciyər Xəstəliyi (NAFLD) və Keton Gövdəsi Metabolizması
Obezite ilə əlaqəli NAFLD və alkoqolsuz steatohepatit (NASH), Qərb ölkələrində qaraciyər xəstəliyinin ən çox görülən səbəbləridir (Rinella və Sanyal, 2016) və NASH səbəb olduğu qaraciyər çatışmazlığı qaraciyər transplantasiyasının ən ümumi səbəblərindən biridir. Hepatositlərdə triasilqliserolların çox miqdarda qaraciyər çəkisinin 5% -də (NAFL) saxlanması degenerativ qaraciyər funksiyasına səbəb olmadığına baxmayaraq, insanlarda NAFLD-a doğru irəliləməsi sistem insulin müqaviməti və tip 2 diabet riskinin artması ilə əlaqələndirir və patogenezinə səbəb ola bilər. ürək-damar xəstəliyi və xroniki böyrək xəstəliyi (Fabbrini və digərləri, 2009; Targher və digərləri, 2010; Targher və Byrne, 2013). NAFLD və NASH-nin patogen mexanizmləri tam başa düşülməmişdir, lakin hepatosit metabolizmasının, hepatosit otofajiyasının və endoplazmik retikulum stresinin, qaraciyərin immun hüceyrələrinin fəaliyyətinin, yağ toxumasının iltihabının və sistemli iltihab vasitəçilərinin anormallıqlarını əhatə edir (Fabbrini və digərləri, 2009; Masuoka və Chalasani, 2013). ; Targher et al., 2010; Yang et al., 2010). Karbohidrat, lipid və amin turşusu metabolizmasının pozulması insanlarda və model orqanizmlərdə obezlik, diabet və NAFLD-də meydana gəlir və bunlara kömək edir [nəzərdən keçirildi (Farese və digərləri, 2012; Lin və Accili, 2011; Newgard, 2012; Samuel və Shulman, 2012; Sun and Lazar, 2013)]. Sitoplazmik lipid mübadiləsindəki hepatosit anormallikleri NAFLD-də (Fabbrini et al., 2010b) tez-tez müşahidə olunsa da, yağların oksidləşdirici atılmasını idarə edən mitokondrial metabolizmanın rolu NAFLD patogenezində daha az aydın görünür. Mitokondrial metabolizma anormallikleri NAFLD / NASH patogenezində meydana gəlir və bunlara kömək edir (Hyotylainen et al., 2016; Serviddio et al., 2011; Serviddio et al., 2008; Wei et al., 2008). Ümumi (Felig vd., 1974; Iozzo vd., 2010; Koliaki vd., 2015; Satapati vd., 2015; Satapati vd., 2012; Sunny vd., 2011) vahid deyil ( Koliaki və Roden, 2013; Perry və digərləri, 2016; Rektor və digərləri, 2010) vicdanlı NASH, qaraciyər mitokondrial oksidləşmə və xüsusilə yağ oksidləşməsinin inkişafından əvvəl obezlik, sistemik insulin müqavimətində artdığına dair bir fikir birliyi. və NAFLD. Çox güman ki, NAFLD irəlilədikcə, fərdi mitokondriyalar arasında da oksidləşdirici qabiliyyət heterogenliyi ortaya çıxır və nəticədə oksidləşdirici funksiya pozulur (Koliaki və digərləri, 2015; Rektor və digərləri, 2010; Satapati və ark., 2008; Satapati və ark. ., 2012).
Ketogenez tez-tez qaraciyər yağının oksidləşməsi üçün bir vasitə kimi istifadə olunur. Ketogenez pozğunluqları heyvan modellərində və ehtimal ki, insanlarda NAFLD irəlilədikcə ortaya çıxır. Natamam müəyyən edilmiş mexanizmlər vasitəsilə hiperinsulinemiya ketogenezi yatırır, ehtimal ki, arıq nəzarətlərlə müqayisədə hipoketonemiyaya kömək edir (Bergman və digərləri, 2007; Bickerton və digərləri, 2008; Satapati et al., 2012; Soeters et al., 2009; , 2011; Vice et al., 2005). Buna baxmayaraq, dövran edən keton cisim konsentrasiyalarının NAFLD-ni proqnozlaşdırmaq qabiliyyəti mübahisəlidir (Münnist et al., 2015; Sanyal et al., 2001). Heyvan modellərində güclü kəmiyyət maqnit rezonans spektroskopik üsulları orta insulin müqaviməti ilə keton dövriyyəsinin sürətini artırdı, lakin daha şiddətli insulin müqaviməti ilə azalma dərəcələri aşkar edildi (Satapati və digərləri, 2012; Sunny və digərləri, 2010). Yağlı qaraciyəri olan obez insanlarda ketogenik nisbət normaldır (Bickerton et al., 2008; Sunny et al., 2011) və buna görə də, ketogenez dərəcələri hepatositlərdə artan yağ turşusu yükü ilə müqayisədə azalır. Nəticə etibarilə, ?-oksidləşmədən əldə edilən asetil-KoA TCA dövründə terminal oksidləşməyə yönəldilə bilər, terminal oksidləşməni, anapleroz/katapleroz və oksidləşdirici stress vasitəsilə fosfoenolpiruvatla idarə olunan qlükoneogenezi artırır. Asetil-KoA, həmçinin lipogenez üçün bir öncül substrat olan sitrat kimi mitoxondriyadan ixraca məruz qalır (Şəkil 4) (Satapati et al., 2015; Satapati et al., 2012; Solinas et al., 2015). Ketogenez insulinə və ya uzun müddətli piylənmə ilə oruc tutmağa daha az cavab versə də (Satapati və digərləri, 2012), bunun əsas mexanizmləri və aşağı axın nəticələri hələ də tam başa düşülməmişdir. Son sübutlar göstərir ki, mTORC1 ketogenezi insulin siqnalının aşağı axınında (Kucejova və s., 2016) yatırır ki, bu da mTORC1-in PPAR?-vasitəçiliyi ilə Hmgcs2 induksiyasını maneə törətdiyinə dair müşahidələrə uyğundur (Sengupta et al., 2010) həmçinin HMGCS2 və SCOT/OXCT1 Qaydalarına baxın).

Qrupumuzun ilkin müşahidələri ketogenik çatışmazlığın mənfi qaraciyər nəticələrini təklif edir (Cotter et al., 2014). Ketogenezin pozulmuş, hətta karbohidratla zəngin və beləliklə, "ketogen olmayan" vəziyyətlərdə belə, anormal qlükoza metabolizminə töhfə verdiyi və steatohepatitə səbəb olduğu fərziyyəsini yoxlamaq üçün hədəflənmiş antisens oliqonukleotidlərin (ASO) tətbiqi ilə qeyd olunan ketogenik çatışmazlığın siçan modelini yaratdıq. Hmgcs2. Standart az yağlı yeməklə qidalanan yetkin siçanlarda HMGCS2-nin itirilməsi mülayim hiperqlikemiyaya səbəb oldu və yüzlərlə qaraciyər metabolitinin istehsalını nəzərəçarpacaq dərəcədə artırdı, bunların bir qrupu lipogenezin aktivləşməsini güclü şəkildə təklif etdi. Qeyri-kafi ketogenezi olan siçanların yüksək yağlı pəhriz ilə qidalanması geniş hepatosit zədəsi və iltihabı ilə nəticələndi. Bu tapıntılar mərkəzi fərziyyələri dəstəkləyir ki, (i) ketogenez passiv daşqın yolu deyil, əksinə qaraciyər və inteqrasiya olunmuş fizioloji homeostazda dinamik bir düyündür və (ii) NAFLD/NASH və pozulmuş qaraciyər qlükoza mübadiləsini azaltmaq üçün ehtiyatlı ketogenik artım tədqiqə layiqdir. .
Zədələnmiş ketogenez qaraciyər zədələnməsinə və qlükoza homeostazının dəyişməsinə necə kömək edə bilər? Birinci məsələ, günahkarın ketogenik axının çatışmazlığı və ya ketonların özləri olub-olmamasıdır. Son bir hesabat, keton cisimlərinin n-3 poli doymamış yağ turşularına cavab olaraq oksidləşdirici stress səbəb olduğu qaraciyər zədəsini azalda biləcəyini təklif edir (Pawlak et al., 2015). Xatırladaq ki, hepatositlərdə SCOT ifadəsinin olmaması səbəbindən keton cisimləri oksidləşmir, lakin onlar lipogenezdə iştirak edə bilir və oksidləşmələrindən asılı olmayaraq müxtəlif siqnal rollarını yerinə yetirə bilirlər (həmçinin keton cisimlərinin və ?OHB-nin oksidləşdirici olmayan metabolik taleyinə baxın). siqnal vasitəçisi). Həm də mümkündür ki, hepatositlərdən əldə edilən keton cisimcikləri, ulduzvari hüceyrələr və Kupffer hüceyrə makrofaqları da daxil olmaqla, qaraciyər asinusunda qonşu hüceyrə növləri üçün siqnal və/yaxud metabolit rolunu oynaya bilər. Mövcud olan məhdud ədəbiyyat makrofaqların keton cisimlərini oksidləşdirə bilmədiyini təklif etsə də, bu, yalnız klassik metodologiyalardan istifadə etməklə və yalnız peritoneal makrofaqlarda ölçülmüşdür (Newsholme et al., 1986; Newsholme et al., 1987), bu, təkrar sümük iliyindən əldə edilən makrofaqlarda bol SCOT ifadəsi nəzərə alınmaqla qiymətləndirmə məqsədəuyğundur (Youm et al., 2015).
Hepatositlərin ketogenik axını da sitoprotektiv ola bilər. Faydalı mexanizmlər özlüyündə ketogenezdən asılı olmasa da, aşağı karbohidratlı ketogenik pəhrizlər NAFLD-nin yaxşılaşdırılması ilə əlaqələndirilmişdir (Browning və digərləri, 2011; Foster və digərləri, 2010; Kani və digərləri, 2014; Schugar və Crawford, 2012) . Müşahidələrimiz göstərir ki, hepatosit ketogenez TCA dövrü axını, anaplerotik axını, fosfoenolpiruvatdan əldə edilən qlükoneogenezi (Cotter və digərləri, 2014) və hətta qlikogen dövriyyəsini əks etdirə və tənzimləyə bilər. Ketogenik pozğunluq asetil-KoA-nı TCA axını artırmağa istiqamətləndirir, bu da qaraciyərdə ROS-vasitəçiliyi ilə zədələnmənin artması ilə əlaqələndirilir (Satapati et al., 2015; Satapati et al., 2012); karbonun sitotoksik olduğunu sübut edə bilən de novo sintez edilmiş lipid növlərinə çevrilməsinə məcbur edir; və NADH-nin NAD+-a yenidən oksidləşməsinin qarşısını alır (Cotter et al., 2014) (Şəkil 4). Birlikdə götürdükdə, nisbi ketogenik çatışmazlığın uyğunlaşa bilməməsi, hiperqlikemiyaya səbəb ola biləcəyi, steatohepatitə səbəb ola biləcəyi mexanizmləri və bu mexanizmlərin insan NAFLD/NASH-də işlək olub-olmadığını həll etmək üçün gələcək təcrübələr tələb olunur. Epidemioloji sübutlar steatohepatitin irəliləməsi zamanı pozulmuş ketogenezin olduğunu göstərir (Embade və s., 2016; Marinou və digərləri, 2011; M�nnist� və digərləri, 2015; Pramfalk və digərləri, 2015; Safaei və digərləri, 2016) qaraciyər ketogenezini artıran müalicələr faydalı ola bilər (Degirolamo et al., 2016; Honda et al., 2016).
Keton cisimləri və ürək çatışmazlığı (HF)
Gündə 400 kkal/kq-dan çox metabolik sürət və 6-35 kq ATP/gün dövriyyəsi ilə ürək ən yüksək enerji sərfiyyatı və oksidləşdirici tələbat olan orqandır (Ashrafian et al., 2007; Wang et al., 2010b). Miokardın enerji dövriyyəsinin böyük əksəriyyəti mitoxondriyaların daxilindədir və bu təchizatın 70%-i FAO-dan qaynaqlanır. Ürək normal şəraitdə hərtərəfli və çevikdir, lakin patoloji olaraq yenidən qurulan ürək (məsələn, hipertoniya və ya miokard infarktı səbəbindən) və diabetik ürək metabolik olaraq elastik olur (Balasse və Fery, 1989; BING, 1954; Fukao et al., 2004). ; Lopaschuk və başqaları, 2010; Taegtmeyer və başqaları, 1980; Taegtmeyer və başqaları, 2002; Young və başqaları, 2002). Həqiqətən, siçan modellərində ürək yanacaq mübadiləsinin genetik olaraq proqramlaşdırılmış anormallikləri kardiomiopatiyaya səbəb olur (Carley et al., 2014; Neubauer, 2007). Fizioloji şəraitdə normal ürəklər keton cisimlərini yağ turşusu və qlükoza oksidləşməsi hesabına onların çatdırılmasına mütənasib olaraq oksidləşdirir və miyokard kütlə vahidinə düşən ən yüksək keton cisim istehlakçısıdır (BING, 1954; Crawford et al., 2009; GARLAND et al. ., 1962; Hasselbaink və başqaları, 2003; Jeffrey və başqaları, 1995; Pelletier və başqaları, 2007; Tardif və başqaları, 2001; Yan və başqaları, 2009). Yağ turşularının oksidləşməsi ilə müqayisədə keton cisimləri enerji baxımından daha səmərəlidir və yatırılan oksigen molekulu başına ATP sintezi üçün daha çox enerji verir (P/O nisbəti) (Kashiwaya et al., 2010; Sato et al., 1995; Veech, 2004) . Keton bədəninin oksidləşməsi həmçinin FAO ilə müqayisədə potensial olaraq daha yüksək enerji verir, ubiquinonu oksidləşmiş saxlayır, bu da elektron daşıma zəncirində redoks intervalını artırır və ATP-ni sintez etmək üçün daha çox enerji verir (Sato et al., 1995; Veech, 2004). Keton cisimlərinin oksidləşməsi də ROS istehsalını və beləliklə, oksidləşdirici stressi azalda bilər (Veech, 2004).
İnterventional və müşahidə edilən tədqiqatlar qəlbdə keton orqanlarının potensial saliyyətli rolunu göstərir. Eksperimental iskemi / reperfüzyon zədə kontekstində, poton potensial kardioprotektiv effektləri (Əl-Zaid və s., 2007; Wang et al., 2008), ehtimal ki, ürəyin mitokondriyal bolluğunun artması və ya həlledici oksidləşdirici fosforiliyin mediatorlar (Snorek və s., 2012; Zou et al., 2002). Son tədqiqatlar göstərir ki, insanlarda əvvəlki müşahidələrin dəstəklənməsi (BING, 2016; Fukao et al., 2016; s.), Siçovulların qəlbində (Aubert və s., 1954) və insanlarda (Bedi et al., 2000) Janardhan et al., 2011, Longo və digərləri, 2004, Rudolph və Schinz, 1973, Tildon və Cornblath, 1972). Dolaşım təzyiqlərinə doğrudan nisbətdə, mexanizmi və əhəmiyyəti bilinməyən müşahidələr (Kopari və s., 1995; Lommi et al., 1996; Lommi et al., 1997; Neely et al ., 1972), lakin kardiyomiyositlərdə seçici SCOT çatışmazlığı olan siçanlar cərrahiyə bağlı olaraq təzyiqə səbəb olan təzyiqə ziyan vurulmasına (Schugar et al., 2014) cavab verən sürətli patoloji ventrikulyar remodeling və ROS imza sərgiləyirlər.
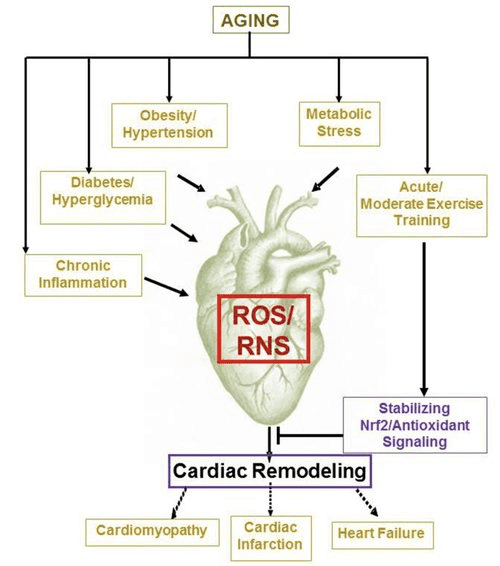
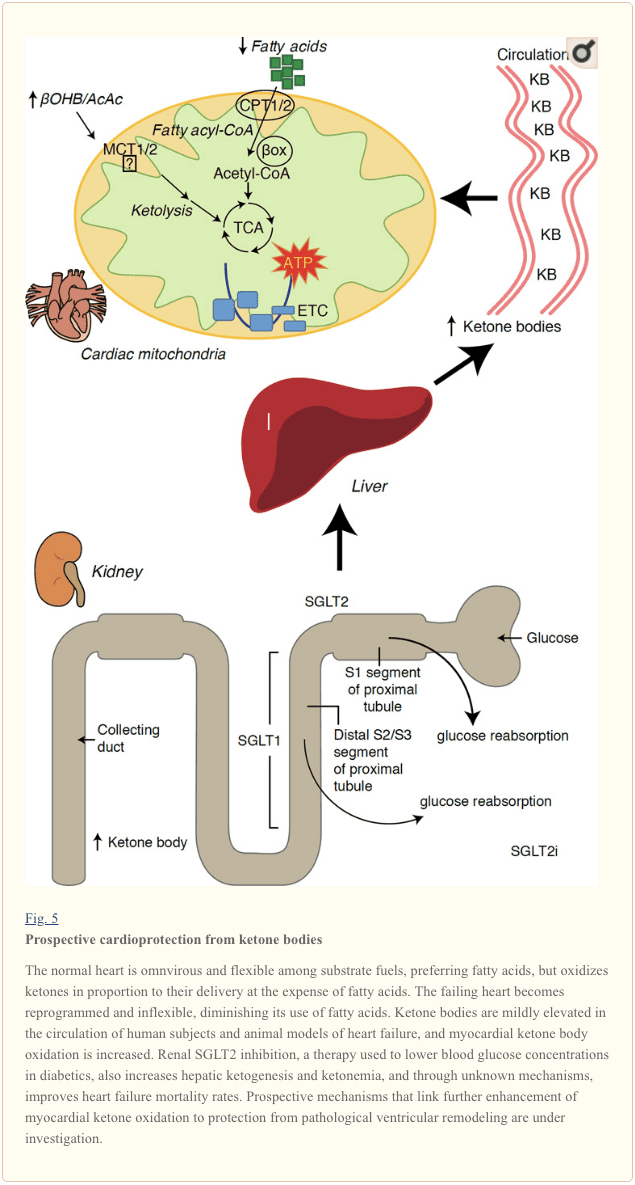
Diabet müalicəsində son zamanlardakı maraqlı müşahidələr miyokardiyal keton metabolizması və patoloji ventrikulyar remodeling arasında potensial bir əlaqə ortaya qoymuşdur (Şəkil 5). böyrək proksimal boru natrium / qlükoza co-yük 2 (SGLT2i) inhibe insanlarda keton bədən konsentrasiyası dövriyyə artırır (Ferrannini et al, 2016a.. Inagaki et al, 2015) və siçan (Suzuki et al, 2014.) artıb vasitəsilə hepatik ketogenez (Ferrannini və digərləri, 2014, Ferrannini və digərləri, 2016a; Katz və Leiter, 2015, Mudaliar və digərləri, 2015). Çox təəssüf ki, bu agentlərin ən azı biri HF-nin xəstəxanaya yerləşdirilməsini azaldıb (məsələn, EMPA-REG OUTCOME sınaqdan çıxarılan kimi) və təkmilləşdirilmiş kardiovaskulyar ölüm (Fitchett və s., 2016; Sonesson et al., 2016; Wu et al., 2016a Zinman et al., 2015). SGLT2i ilə əlaqəli faydalı HF nəticələri arxasında sürücülük mexanizmləri aktual olaraq müzakirə olunur, baxmayaraq ki, sağalma fayda potensial, potensial olaraq ketoz, o cümlədən çəki, qan təzyiqi, qlükoza və ürik turşusu səviyyələrinə, arteriya sərtliyinə, simpatik sinir sisteminə, ozmotik Diurez / azaldılmış plazma həcmi və artmış hematokrit (Raz və Cahn, 2016, Vallon və Thomson, 2016). HF xəstələrində və ya HF inkişaf etdirmək üçün yüksək riskli xəstələrdə terapötik olaraq artan ketonemiyanın olduğu mülahizələr hələ də mübahisəli olaraq qalır, lakin klinik və klinik tədqiqatlarda aktiv araşdırma aparılır (Ferrannini və s., 2016b; Kolwicz et al. 2016, Lopaschuk və Verma, 2016; Mudaliar və s., 2016; Taegtmeyer, 2016).
Xərçəng Biologiyasında Keton Bədənləri
Keton cisimləri və xərçəng arasında əlaqələr sürətlə inkişaf edir, lakin heyvan modellərində və insanlarda araşdırmalar müxtəlif nəticələr verir. Keton metabolizması dinamik və qidalı vəziyyətə sahib olduğundan, həssaslıqla idarə olunan qidalanma müalicəsi potensialı səbəbindən xərçəngə bioloji əlaqələri davam etdirməyi təqdir edir. Xərçəng hüceyrələri sürətli hüceyrələrin yayılmasının və böyüməsinin (DeNicola və Cantley, 2015, Pavlova və Thompson, 2016) qorumaq üçün metabolik reprogramminqdən keçir. Xərçəng hüceyrələrinin maddələr mübadiləsində klassik Warburg təsiri enerji ötürmək və oksidləşdirici fosforiliya və məhdud mitokondrial tənəffüsündən daha az asılılığı ödəmək üçün glikoliz və laktik turşu fermentasiyasının dominant rolundan yaranır (De Feyter və s., 2016; Grabacka et al., 2016; Kang et al., 2015; Poff et al., 2014; Shukla və digərləri, 2014). Glyukoza karbonu, əsasən, glycolysis, pentoz fosfat yolu və lipogenezi ilə yönəldilir ki, bu da şişlərin biyokütlə genişləndirilməsi üçün zəruri vasitədir (Grabacka və s., 2016; Shukla və s., 2014; Yoshii et al., 2015). Xərçəng hüceyrələrinin qlükoza deprivasiyasına uyğunlaşdırılması asetat, glutamin və aspartat daxil olmaqla alternativ yanacaq mənbələrinin istifadəsi qabiliyyətindən yaranır (Jaworski və s., 2016; Sullivan et al., 2015). Məsələn, pyruvatata məhdud giriş xərçəng hüceyrələrinin acetil-Koa-ya glutamini karboksilyasiyaya çevirmək qabiliyyətini ortaya qoyur, həm də enerjili və anabolik ehtiyacları saxlayır (Yang və s., 2014). Xərçəng hüceyrələrinin maraqlı bir adaptasiyası yanacaq olaraq asetatın istifadə edilməsidir (Comerford və s., 2014; Jaworski və s., 2016; Mashimo və s., 2014; Wright and Simone, 2016; Yoshii et al., 2015). Acetate də şiş hüceyrələrinin yayılması üçün kritik olan lipogenez üçün substratdır və bu lipojenik kanalın əldə edilməsi daha qısa xəstə sağkalımı və daha böyük şiş yükü ilə əlaqələndirilir (Comerford və s., 2014; Mashimo et al., 2014; Yoshii et al ., 2015).
Xərçəng olmayan hüceyrələr qlükoza çatışmazlığı zamanı enerji mənbəyini qlükozadan keton cisimlərinə asanlıqla köçürür. Bu plastiklik xərçəng hüceyrələrinin növləri arasında daha dəyişkən ola bilər, lakin in vivo implantasiya edilmiş beyin şişləri ətrafdakı beyin toxuması ilə oxşar dərəcədə oksidləşir [2,4-13C2]-?OHB (De Feyter et al., 2016). "Tərs Warburq effekti" və ya "iki bölməli şiş metabolizması" modelləri, xərçəng hüceyrələrinin bitişik fibroblastlarda OHB istehsalını induksiya etdiyini və şiş hüceyrəsinin enerji ehtiyacını təmin etdiyini fərz edir (Bonuccelli və digərləri, 2010; Martinez-Outschoorn et al., 2012) . Qaraciyərdə hepatositlərin hepatosellüler karsinoma (hepatoma) hüceyrələrində ketogenezdən keton oksidləşməsinə keçməsi iki hepatoma hüceyrə xəttində müşahidə olunan BDH1 və SCOT fəaliyyətlərinin aktivləşməsi ilə uyğun gəlir (Zhang və digərləri, 1989). Həqiqətən, hepatoma hüceyrələri OXCT1 və BDH1-i ifadə edir və ketonları oksidləşdirir, ancaq serum ac qaldıqda (Huang et al., 2016). Alternativ olaraq, şiş hüceyrələrinin ketogenezi də təklif edilmişdir. Ketogen gen ifadəsində dinamik dəyişikliklər, normal olaraq HMGCS2-ni ifadə edən bir hüceyrə növü olan kolon epitelinin xərçəng transformasiyası zamanı nümayiş etdirilir və son hesabatda HMGCS2-nin kolorektal və skuamöz hüceyrəli karsinomalarda pis proqnozun proqnostik markeri ola biləcəyi irəli sürülür (Camarero et al., 2006; Chen və başqaları, 2016). Bu assosiasiyanın ketogenezi və ya HMGCS2-nin ay işığı funksiyasını tələb edib etmədiyini müəyyən etmək qalır. Əksinə, PPAR tərəfindən stimullaşdırılan melanoma və glioblastoma hüceyrələri tərəfindən aydın ?OHB istehsalı? agonist fenofibrat, böyümənin dayandırılması ilə əlaqəli idi (Grabacka et al., 2016). Xərçəng hüceyrələrində HMGCS2/SCOT ifadəsi, ketogenez və keton oksidləşməsinin rollarını xarakterizə etmək üçün əlavə tədqiqatlar tələb olunur.
Yanacaq mübadiləsi sahəsindən kənarda, ketonlar son zamanlarda bir siqnal mexanizmi vasitəsilə xərçəng hüceyrələrinin biologiyasına aid edilmişdir. BRAF-V600E+ melanomasının təhlili HMGCL-nin OCT1-dən asılı induksiyasını onkogenik BRAF-dan asılı şəkildə göstərdi (Kang et al., 2015). HMGCL artımı daha yüksək hüceyrə AcAc konsentrasiyası ilə əlaqələndirildi, bu da öz növbəsində BRAFV600E-MEK1 qarşılıqlı təsirini artıraraq, şiş hüceyrələrinin yayılmasını və böyüməsini sürətləndirən irəli ötürücü döngədə MEK-ERK siqnalını gücləndirdi. Bu müşahidələr daha sonra siqnal mexanizmini dəstəkləyən perspektivli ekstrahepatik ketogenezlə bağlı maraqlı sualı qaldırır (həmçinin bax: ?OHB siqnal vasitəsi kimi və ekstrahepatik ketogenezdə mübahisələr). AcAc, d-?OHB və l-?OHB-nin xərçəng metabolizminə müstəqil təsirlərini nəzərə almaq da vacibdir və HMGCL-ni nəzərdən keçirərkən, lösin katabolizmi də pozula bilər.
Xərçəng heyvan modellərində ketogenik diyetlərin (həmçinin ketogenik pəhrizin və ekzogen keton cisimlərinin terapevtik istifadəsi) təsirləri müxtəlifdir (De Feyter və digərləri, 2016; Klement və digərləri, 2016; Meidenbauer və digərləri, 2015; Poff et al. ., 2014; Seyfried və başqaları, 2011; Shukla et al., 2014). Piylənmə, xərçəng və ketogenik diyetlər arasında epidemioloji assosiasiyalar müzakirə edilərkən (Liskiewicz et al., 2016; Wright and Simone, 2016), heyvan modellərində və insan tədqiqatlarında ketogenik pəhrizlərdən istifadə edən meta-analiz, sağ qalmağa müsbət təsir göstərdiyini irəli sürdü. ketozun böyüklüyü, pəhrizin başlama vaxtı və şiş yeri ilə əlaqəli faydalar (Klement et al., 2016; Woolf et al., 2016). Pankreas xərçəngi hüceyrələrinin keton cisimləri (d-?OHB və ya AcAc) ilə müalicəsi böyüməni, yayılmasını və qlikolizi inhibə etdi və ketogenik pəhriz (81% kkal yağ, 18% protein, 1% karbohidrat) in vivo şişin çəkisini, qlikemiyanı və azaldıb. implantasiya edilmiş xərçəngi olan heyvanlarda artan əzələ və bədən çəkisi (Shukla et al., 2014). Oxşar nəticələr pəhrizdə keton əlavəsi alan siçanlarda metastatik qlioblastoma hüceyrə modelindən istifadə etməklə müşahidə edilmişdir (Poff et al., 2014). Əksinə, ketogenik pəhriz (91% kkal yağ, 9% protein) dövran edən OHB konsentrasiyasını artırdı və qlikemiyanı azaltdı, lakin glioma daşıyan siçovullarda nə şiş həcminə, nə də sağ qalma müddətinə təsir göstərmədi (De Feyter et al., 2016). Qlükoza keton indeksi insanlarda və siçanlarda ketogenik diyetə səbəb olan beyin xərçəngi müalicəsinin metabolik idarəçiliyini yaxşılaşdıran klinik göstərici kimi təklif edilmişdir (Meidenbauer et al., 2015). Birlikdə götürdükdə, keton cisimlərinin metabolizması və keton cisimlərinin xərçəng biologiyasındakı rolları cəlbedicidir, çünki onların hər biri uyğun müalicə variantları yaradır, lakin (i) ekzogen keton arasındakı fərqlər də daxil olmaqla, dəyişənlər matrisindən yaranan aydın təsirlərlə əsas aspektlər hələ də aydınlaşdırılmalıdır. orqanlar ketogenik pəhrizə qarşı, (ii) xərçəng hüceyrə növü, genomik polimorfizmlər, dərəcə və mərhələ; və (iii) ketotik vəziyyətə məruz qalma vaxtı və müddəti.

Ketogenez yağlı turşuların və ketojenik amin turşularının parçalanması yolu ilə keton orqanları tərəfindən yaradılır. Bu biyokimyəvi proses qan qlükoza çatışmazlığına cavab olaraq oruc tutma şəraitində müxtəlif orqanlara, xüsusən beynə enerji verir. Keton cəsədləri əsasən qaraciyər hüceyrələrinin mitokondriyalarında istehsal olunur. Digər hüceyrələr ketogenezi aparmaq qabiliyyətinə malik olsa da, onlar qaraciyər hüceyrələri kimi effektiv olmurlar. Ketogenez mitokondriyada meydana gəldiyindən, prosesləri müstəqil şəkildə tənzimlənir. Dr. Alex Jimenez DC, CCST Insight
Ketojenik Diyet və Exogen Keton Cisimlərinin Müalicəvi tətbiqi
Ketogenik diyetlərin və keton cisimlərinin terapevtik vasitələr kimi tətbiqləri, piylənmə və NAFLD/NASH daxil olmaqla, xərçəngli olmayan kontekstlərdə də yaranmışdır (Browning et al., 2011; Foster et al., 2010; Schugar and Crawford, 2012); ürək çatışmazlığı (Huynh, 2016; Kolwicz et al., 2016; Taegtmeyer, 2016); nevroloji və neyrodegenerativ xəstəlik (Martin və digərləri, 2016; McNally və Hartman, 2012; Rho, 2015; Rogawski və digərləri, 2016; Yang və Cheng, 2010; Yao və digərləri, 2011); maddələr mübadiləsinin anadangəlmə səhvləri (Scholl-B�rgi et al, 2015); və məşq performansı (Cox et al., 2016). Ketogenik pəhrizlərin effektivliyi xüsusilə dərmana davamlı xəstələrdə epileptik tutmaların müalicəsində yüksək qiymətləndirilmişdir. Əksər tədqiqatlar pediatrik xəstələrdə ketogenik pəhrizləri qiymətləndirdi və seçilmiş sindromlarda effektivliyin yaxşılaşması ilə 50 aydan sonra tutma tezliyində ~ 3% -ə qədər azalma aşkar etdi (Wu et al., 2016b). Təcrübə böyüklər epilepsiyasında daha məhduddur, lakin simptomatik ümumiləşdirilmiş epilepsiya xəstələrində daha yaxşı cavab verən oxşar azalma göz qabağındadır (Nei et al., 2014). Qlükoza istifadəsi/qlikolizinin azalması, yenidən proqramlaşdırılmış qlutamat daşınması, ATP-həssas kalium kanalına və ya adenozin A1 reseptoruna dolayı təsir, natrium kanalının izoform ifadəsinin dəyişməsi və ya dövran edən hormonlara təsir (o cümlədən, əsas antikonvulsant mexanizmlər aydın deyildir) Lambrechts et al., 2016; Lin et al., 2017; Lutas and Yellen, 2013). Anti-konvulsant təsirin ilk növbədə keton cisimlərinə, yoxsa aşağı karbohidratlı diyetlərin kaskad metabolik nəticələrinə görə olub-olmaması aydın deyil. Buna baxmayaraq, keton esterləri (aşağıya bax) təhrik edilmiş nöbetlərin heyvan modellərində tutma həddini yüksəldir (Ciarlone və digərləri, 2016; D'Agostino və digərləri, 2013; Viggiano et al., 2015).
Atkins-stil və ketogenic, aşağı karbohidrat diyeti tez-tez xoşagəlməz hesab olunur, və (Bisschop et al Hyperglycemia səbəb və xolesterol və pulsuz yağ turşusu konsentrasiyası dövriyyə qaldırmaq qəbizlik, hyperuricemia, hipokalsemi hypomagnesemia, sidik səbəb, ketoasidozu səbəb ola bilər. 2001 Kossoff və Hartman, 2012, Kwiterovich və digərləri, 2003, Suzuki və s., 2002). Bu səbəblərə görə uzunmüddətli sadiqlik problemlər yaradır. Rodent tədqiqatları güclü bir ketoza səbəb olan fərqli makronutrient dağılımını (94% kkal yağ, 1% kcal karbohidrat, 5% kcal protein, Bio-Serv F3666) istifadə edir. Bununla birlikdə, xNUMX% kcal hətta protein məzmununun artırılması ketozu əhəmiyyətli dərəcədə azaldır və 10% kkal protein məhdudlaşdırılması metabolik və fizioloji təsirləri qarışdırır. Bu pəhriz formulasiyasında da kolin tükəndi, qaraciyər zədələnməsinə və hətta ketojenezə təsir edən bir dəyişən (Garbow və s., 5; Jornayvaz et al., 2011; Kennedy et al., 2010; Pissios et al., 2007; Schugar və s., 2013). Sətrin tərkibində ketojenik diyetlərin uzunmüddətli istifadəsinin təsiri tam olaraq müəyyən edilməmişdir, lakin siçandakı son tədqiqatlar amin turşu metabolizması, enerji xərcləri və insulin siqnalları olmasına baxmayaraq, sətrin tərkibində ketogenic dietlərdə siçovulların qaraciyər zədələnmə markalarının olmamasıdır olduqca reprogrammed (Douris və s., 2013).
Ketogenik dietaya alternativ mexanizmlər vasitəsilə ketozin artması mexanizmləri içilməkdə olan keton vücudunun prekursorlarının istifadəsini nəzərdə tutur. Ekzogen keton orqanlarının idarəsi normal fizyoloji ilə qarşılaşmayan nadir fizioloji vəziyyət yarada bilər, çünki hüceyrələr qlükoza alışını və istifadəsini ehtiyatla saxlaya bilər, çünki glyukoza və insulin dövranı nisbətən normaldır. Keton cisimlərinin yarı ömrü qısadır və terapevtik ketoza nail olmaq üçün natrium-OHB duzunun qəbulu və ya infuziyası arzuolunmaz natrium yüklənməsinə səbəb olur. R/S-1,3-butandiol qaraciyərdə asanlıqla oksidləşərək d/l-?OHB əldə edən qeyri-toksik dialkoldur (Desrochers et al., 1992). Fərqli eksperimental kontekstlərdə bu doza yeddi həftə ərzində siçanlara və ya siçovullara gündəlik tətbiq edilib və bu doza tətbiq edildikdən sonra 5 saat ərzində 2 mM-ə qədər dövran edən OHB konsentrasiyaları verir, bu da ən azı əlavə 3 saat (D') stabildir. Agostino et al., 2013). R / S-1,3-butanediol (Carpenter və Grossman, 1983) verilmiş gəmiricilərdə qida qəbulunun qismən dayandırılması müşahidə edilmişdir. Bundan əlavə, üç kimyəvi cəhətdən fərqli keton efirləri (KE), (i) R-1,3-butandiol və d-?OHB (R-3-hidroksibutil R-?OHB) monoesteri; (ii) qliseril-tris-?OHB; və (iii) R,S-1,3-butanediol asetoasetat diester də geniş şəkildə tədqiq edilmişdir (Brunengraber, 1997; Clarke et al., 2012a; Clarke et al., 2012b; Desrochers et al., 1995a Desrochers et al.; ., 1995b; Kashiwaya et al., 2010). Birincinin xas üstünlüyü ondan ibarətdir ki, bağırsaqda və ya qaraciyərdə esterazanın hidrolizindən sonra hər mol KE üçün 2 mol fizioloji d-?OHB əmələ gəlir. Təhlükəsizlik, farmakokinetik və tolerantlıq ən geniş şəkildə R-3-hidroksibutil R-?OHB-ni 714 mq/kq-a qədər dozada qəbul edən insanlarda tədqiq edilmişdir, dövriyyədə 6 mM-ə qədər olan d-?OHB konsentrasiyası əldə edilmişdir (Clarke et al., 2012a; Cox və digərləri, 2016; Kemper və başqaları, 2015; Shivva və başqaları, 2016). Kemiricilərdə bu KE kalorili suqəbuledici və plazma ümumi xolesterini azaldır, qəhvəyi yağ toxumasını stimullaşdırır və insulinə qarşı müqaviməti yaxşılaşdırır (Kashiwaya və digərləri, 2010; Kemper et al., 2015; Veech, 2013). Son tapıntılar göstərir ki, təlim keçmiş idmançılarda məşq zamanı R-3-hidroksibutil R-?OHB qəbulu skelet əzələsi qlikolizinin və plazma laktat konsentrasiyasının azalmasına, əzələdaxili triaçilqliserol oksidləşməsinin artmasına və hətta karbohidratın birgə qəbulu (insulin sekresiyasını stimullaşdırdığı halda) əzələ qlikogeninin saxlanmasına səbəb olur. Cox və başqaları, 2016). Bu maraqlı nəticələrin daha da inkişaf etdirilməsi tələb olunur, çünki dözümlülük idmanının inkişafı əsasən 2 / 8 mövzularında KE-yə möhkəm cavab verilir. Buna baxmayaraq, bu nəticələr digər substratlardan (GARLAND və s., 1962; Hasselbaink et al., 2003; Stanley et al., 2003; Valente-Silva et al., 2015), keton oksidləşmə üstünlüklərini göstərən klassik tədqiqatları dəstəkləyir. (Johnson və digərləri, 1969a; Johnson və Walton, 1972; Winder və s., 1974; Winder və digərləri, 1975). Nəhayət, bərabər kalorili suqəbuledici (fərqli olaraq makronutrientlər arasında paylanmış) və bərabər oksigen istehlakı nisbətlərini nəzərə alaraq təkmilləşdirilmiş həyata keçirmə fəaliyyətini dəstəkləyən mexanizmlər müəyyənləşdirilməlidir.
Gələcək Perspektiv
Bir zamanlar karbohidratla məhdudlaşan dövlətlərdə ("ketotoksik" paradiqma) yağların yanmasından zəhərli emissiyaları toplamaq qabiliyyətinə malik daşqın yolu kimi damğalanmış son müşahidələr, keton cisimlərinin metabolizmasının hətta karbohidratla yüklənmiş vəziyyətdə də faydalı rol oynadığı və ketohormetik təsir göstərdiyi fikrini dəstəkləyir. � fərziyyə. Keton mübadiləsini manipulyasiya etmək üçün asan qidalanma və farmakoloji yanaşmalar onu cəlbedici bir terapevtik hədəfə çevirsə də, həm əsas, həm də tərcümə tədqiqat laboratoriyalarında aqressiv şəkildə qurulmuş, lakin ehtiyatlı təcrübələr qalır. Ürək çatışmazlığı, piylənmə, NAFLD/NASH, tip 2 diabet və xərçəngdə keton mübadiləsindən istifadənin rolunun müəyyən edilməsi sahələrində qarşılanmamış ehtiyaclar meydana çıxdı. Keton cisimlərinin "qeyri-kanonik" siqnal rollarının əhatə dairəsi və təsiri, o cümlədən metabolik və siqnal yollarına irəli və geri qidalanan PTM-lərin tənzimlənməsi daha dərin araşdırma tələb edir. Nəhayət, ekstrahepatik ketogenez maraqlı parakrin və avtokrin siqnal mexanizmlərini və terapevtik məqsədlərə nail olmaq üçün sinir sistemi və şişlərdə ko-metabolizmə təsir etmək imkanlarını aça bilər.
Minnətdarlıq
Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/
Dəyişikliklər
Nəticə olaraq, keton cisimləri insan orqanizmində kifayət qədər qlükoza olmadıqda enerji mənbəyi kimi istifadə olunmaq üçün qaraciyər tərəfindən yaradılır. Ketogenez qanda aşağı qlükoza səviyyəsi olduqda, xüsusən də digər hüceyrə karbohidrat ehtiyatları tükəndikdən sonra baş verir. Yuxarıdakı məqalənin məqsədi keton cisimlərinin yanacaq mübadiləsində, siqnalizasiyada və terapevtikada çoxölçülü rollarını müzakirə etmək idi. Məlumatlarımızın əhatə dairəsi şiroterapi və onurğa sağlamlığı problemləri ilə məhdudlaşır. Mövzunu müzakirə etmək üçün Dr. Jimenezdən soruşun və ya bizimlə əlaqə saxlayın915-850-0900 .
Dr. Alex Jimenez tərəfindən qurulub
İstinad: Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/

Əlavə Mövzu Müzakirəsi: Kəskin Bel Ağrısı
Kürək, bel ağrısıWorldwide dünya miqyasında əlilliyin və işdə buraxılmış günlərin ən çox yayılan səbəblərindən biridir. Bel ağrısı, yalnız yuxarı tənəffüs yoluxucu xəstəliklərin sayından çox olan həkim ofisinə müraciətlərin ikinci ən ümumi səbəbi ilə əlaqələndirilir. Əhalinin təxminən yüzdə 80-i ömrü boyu ən azı bir dəfə bel ağrısı yaşayacaq. Onurğa digər yumşaq toxumaların yanında sümüklərdən, oynaqlardan, bağlardan və əzələlərdən ibarət kompleks bir quruluşdur. Yaralanmalar və / və ya ağırlaşdırılmış şərtlər, məsələnherniated disklər, nəticədə bel ağrısı əlamətlərinə səbəb ola bilər. İdman zədələri və ya avtomobil qəzası xəsarətləri tez-tez bel ağrısının ən çox görülən səbəbidir, lakin bəzən ən sadə hərəkətlər ağrılı nəticələrə səbəb ola bilər. Xoşbəxtlikdən, şiroterapi baxımı kimi alternativ müalicə variantları, onurğa düzəlişləri və əllə manipulyasiya istifadə edərək bel ağrısını azaltmağa kömək edə bilər və nəticədə ağrı kəsicisini yaxşılaşdırır.

EXTRA EXTRA | Vacib Mövzu: Tövsiyə olunan El Paso, TX Chiropractor
***